
根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l)
ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l)
ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g)
ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是( )
A.Q1>Q2>Q3 B.Q1>Q3>Q2
C.Q3>Q2>Q1 D.Q2>Q1>Q3
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:
为省药品和时间,甲、乙、丙三位同学用铜片、锌片、稀硫酸、CuSO4溶液(直流电源、石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器用品)以巧妙的构思“接力”的方式,设计了比较铜与锌金属活动性相对强弱的系列实验。试填写下列空白:
(1)甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),小心向烧杯中加入稀硫酸,观察到的现象是___________________________________________________
________________________________________________________________________。
甲同学的设计思路是__________________________________________________
________________________________________________________________________。
(2)乙同学接着甲的实验,向烧杯中滴加________溶液,进而观察到的现象是________________________________________________________________________
________________________________________________________________________。
乙同学判断出锌、铜金属活动性相对强弱,所依据的原理是
________________________________________________________________________
________________________________________________________________________。
(3)丙同学使用直流电源、石墨电极组装好电解装置,向乙同学实验后的溶液中补充了必要的试剂(作为电解液),反应在调控下随即开始,实验中有关的化学反应方程式为________________________________________________________________________
________________________________________________________________________。
获得的实验明显现象是_______________________________________________
________________________________________________________________________。
(4)请你再单独设计一个简单的实验(试剂、仪器自选),探究和证实锌和铜的金属活动性的相对强弱(简要说明操作和现象)________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。

根据以上条件,回答下列问题:
(1)A与B反应生成C的化学方程式为_______________________________________,
正反应为________(填“吸热”或“放热”)反应。
(2)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有__________(填字母编号)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
科目:初中化学 来源: 题型:
某温度时,N2+3H22NH3的平衡常数K=a,则此温度下,NH33/2H2+1/2N2的平衡常数为( )
A.a-1/2 B.a1/2
C.a D.a-2
查看答案和解析>>
科目:初中化学 来源: 题型:
在下列各说法中,正确的是( )
A.ΔH>0表示放热反应,ΔH<0表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 mol O2反应放出的热就是H2的标准燃烧热
查看答案和解析>>
科目:初中化学 来源: 题型:
以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下:
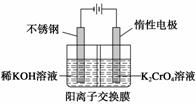
下列说法不正确的是( )
A.在阴极室,发生的电极反应为2H2O+2e-===2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO+2H+Cr2O+H2O向右移动
C.该制备过程中总反应的化学方程式为4K2CrO4+4H2O2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr)为d,则此时铬酸钾的转化率为1-
查看答案和解析>>
科目:初中化学 来源: 题型:
用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加。

(1)写出乙中两极发生的电极反应式。
阴极:________________________________________________________________________;
阳极:________________________________________________________________________。
(2)写出甲中发生反应的化学方程式:___________________________________________。
(3)C(左)、C(右)、Fe、Ag 4个电极上析出或溶解物质的物质的量之比是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
下表提供了A、B两种物质的溶解度数据,读取信息后回答:
| 温 | 0 | 20 | 40 | 60 | 80 | 100 |
| 物质A的 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 |
| 物质B的 溶解度/g | 13.3 | 31.6 | 63.9 |
| 169 | 246 |
(1)A、B物质都属于__________物质(填“难溶”“微溶”“可溶”或“易溶”);
(2)A、B两物质的溶解度随温度 变化趋势的不同是____________________。如下图
变化趋势的不同是____________________。如下图 给出的曲线中,__________________与A物质溶解度的变化趋势相符(填曲线编号);
给出的曲线中,__________________与A物质溶解度的变化趋势相符(填曲线编号);
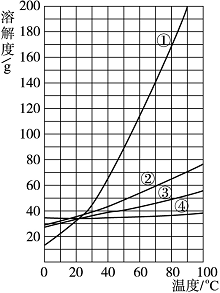
(3)从A、B两物质的混合物中分离出B物质,一般采用______的方法。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com