
分析 (1)根据金属的活动性顺序可以知道,锌铜混合物中铜不能与稀硫酸反应放出氢气,可以据此结合锌和稀硫酸反应的化学方程式进行计算参加反应锌的质量;
(2)根据锌与硫酸反应的化学方程式,由生成氢气的质量可计算恰好完全反应时消耗硫酸的质量,然后结合溶液中溶质的质量分数的计算公式进行解答即可.
(3)根据锌与硫酸反应的化学方程式,由生成氢气的质量可计算恰好完全反应时生成硫酸锌的质量,然后结合溶液中溶质的质量分数的计算公式进行解答即可.
解答 解:(1)设生成0.2g氢气消耗锌的质量为x,消耗硫酸的质量为y,反应后生成硫酸锌的质量为z,
Zn+H2SO4═ZnSO4+H2↑
65 98 161 2
x y z 0.2g
$\frac{65}{x}=\frac{98}{y}=\frac{161}{z}=\frac{2}{0.2g}$
解得:x=6.5g,y=9.8g,z=16.1g
(2)稀硫酸中溶质的质量分数是$\frac{9.8g}{100g}×100%$=9.8%,
(3)反应后所的溶液中溶质的质量分数为:$\frac{16.1g}{100g+6.5g-0.2g}$×100%=15.1%
答:(1)混合物中锌的质量为6.5g
(2)稀硫酸中溶质的质量分数是9.8%,
(3)反应后溶液的溶质质量分数w为15.1%.
点评 根据化学方程式可以表示反应中各物质的质量关系,由反应中一种物质的质量可计算出反应中其它物质的质量.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:初中化学 来源: 题型:实验探究题
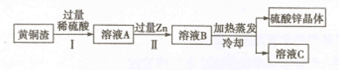
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Zn2+中的“2”表示锌原子带有2个单位的正电荷 | |
| B. | 2NO中的“2”表示2个一氧化氮分子 | |
| C. | H2CO3中的“2”表示一个碳酸分子中含有2个氢元素 | |
| D. | Al2($\stackrel{-2}{SO}$4)3中的“2”表示3个硫酸根离子的化合价为-2价 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
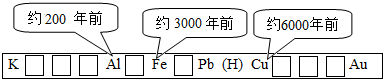
| A. | 金属的化合价高低 | B. | 金属的导电性强弱 | ||
| C. | 金属的活动性强弱 | D. | 金属在地壳中的含量 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
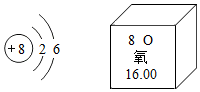 农作物必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等.
农作物必需的营养元素有碳、氢、氧、氮、磷、钾、钙、镁等.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
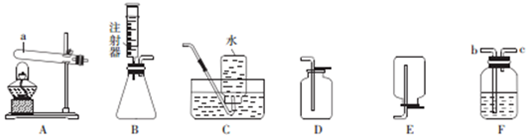
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 原子序数 | 中文名称 | 符号 | 汉语拼音 |
| 113 | 鉨 | Nh | nǐ |
| 115 | 镆 | mò | |
| 117 |  | Ts | tián |
| 118 |  | Og | ào |
| A. | 鉨属于金属元素 | B. | 镆的元素符号是 mo | ||
| C. |  元素的相对原子质量是 117 元素的相对原子质量是 117 | D. |  元素在自然界中含量丰富 元素在自然界中含量丰富 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硅元素在二氧化硅中显+4价 | B. | 呈碱性的物质不一定是碱 | ||
| C. | pH<5.6的降水,属于酸雨 | D. | 通过化学变化可以使黄铜变成黄金 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com