
| A£® | NaCl”¢Fe2£ØSO4£©3 KNO3 | B£® | Al2£ØSO4£©3 NaNO3 NaCl | ||
| C£® | K2CO3 NH4NO3 MgCl2 | D£® | AgNO3 Na2SO4 KCl |
·ÖĪö pHĪŖ2µÄĖ®ČÜŅŗĻŌĖįŠŌ£¬Ė®ČÜŅŗÖŠŗ¬ÓŠ“óĮæµÄH+£®øł¾Żø“·Ö½ā·“Ó¦·¢ÉśµÄĢõ¼žæÉÖŖ£¬ČōĪļÖŹÖ®¼äĻą»„½»»»³É·Ö²»ÄÜÉś³ÉĖ®”¢ĘųĢ唢³Įµķ£¬ŌņÄܹ»ŌŚČÜŅŗÖŠ“óĮæ¹²“ę£®±¾Ģā»¹ŅŖ×¢ŅāÄܵƵ½ĪŽÉ«ČÜŅŗ£¬²»ÄÜŗ¬ÓŠĆ÷ĻŌÓŠŃÕÉ«µÄĶĄė×Ó”¢ĢśĄė×ÓŗĶŃĒĢśĄė×ÓµČ£®
½ā“š ½ā£ŗpHĪŖ2µÄĖ®ČÜŅŗĻŌĖįŠŌ£¬Ė®ČÜŅŗÖŠŗ¬ÓŠ“óĮæµÄH+£®
A”¢ČżÕßÖ®¼ä²»·“Ó¦£¬ĒŅÄÜŌŚĖįŠŌČÜŅŗÖŠ¹²“ę£¬µ«Fe2£ØSO4£©3ČÜÓŚĖ®³Ź»ĘÉ«µÄ£¬¹ŹŃ”Ļī“ķĪó£®
B”¢ČżÕßÖ®¼ä²»·“Ó¦£¬ÄÜŌŚĖįŠŌČÜŅŗÖŠ¹²“ę£¬ĒŅ²»“ęŌŚÓŠÉ«Ąė×Ó£¬¹ŹŃ”ĻīÕżČ·£®
C”¢K2CO3 ÖŠµÄĢ¼ĖįøłĄė×ÓÓėĖįŠŌČÜŅŗÖŠµÄH+Į½ÖÖĄė×ÓÄܽįŗĻ³ÉĖ®ŗĶ¶žŃõ»ÆĢ¼£¬²»ÄÜ“óĮæ¹²“ę£¬²»ÄÜ“óĮæ¹²“ę£¬¹ŹŃ”Ļī“ķĪó£®
D”¢AgNO3ŗĶKClŌŚČÜŅŗÖŠĻą»„½»»»³É·Ö£¬Éś³É²»ČÜÓŚĖįµÄĀČ»ÆŅų³Įµķ£¬²»ÄÜ“óĮæ¹²“ę£¬¹ŹŃ”Ļī“ķĪó£®
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄ¹²“ęĪŹĢā£¬ÅŠ¶ĻĪļÖŹŌŚČÜŅŗÖŠÄÜ·ń¹²“ę£¬Ö÷ŅŖæ“ČÜŅŗÖŠµÄø÷ĪļÖŹÖ®¼äÄÜ·ń·¢Éś·“Ӧɜ³É³Įµķ”¢ĘųĢ唢Ė®£»»¹ŅŖ×¢ŅāŌŚĖįŠŌČÜŅŗÖŠ¹²“ę”¢ĢŲ¶ØĄė×ÓµÄŃÕÉ«£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹĀŹµ»ņĻÖĻó | ½āŹĶ |
| A | ¶žŃõ»ÆĢ¼ŗĶŅ»Ńõ»ÆĢ¼ŠŌÖŹ²»Ķ¬ | Į½ÖÖĪļÖŹµÄŌŖĖŲ×é³ÉĻąĶ¬£¬·Ö×Ó¹¹³É²»Ķ¬ |
| B | ĻÄĢģµÄøßŃ¹ĀĮĻ߱ȶ¬Ģģ³¤ | ĻÄĢģĪĀ¶Čøߣ¬ĀĮŌ×ÓĢå»ż±ä“ó |
| C | ±łĖ®»ģŗĻĪļŹōÓŚ“æ¾»Īļ | ¶¼ŗ¬ÓŠĶ¬ÖÖ·Ö×Ó |
| D | ¼ÓČČŹ±£¬Ė®Õō·¢æģ | Ė®·Ö×ÓŹÜČČ£¬ŌĖ¶ÆĖŁ¶Č¼Óæģ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³öŠŠŹ±³Ė×ų¹«½»³µ»ņ²½ŠŠ | B£® | ½«·Ļ¾ÉµÄĖÜĮĻÖĘĘ·ĢīĀń“¦Ąķ | ||
| C£® | øĽųČ¼ÓĶĘ·ÖŹ£¬¼õÉŁĘū³µĪ²ĘųÅÅ·Å | D£® | ¶ŌŃĻÖŲĪŪČ¾»·¾³µÄĘóŅµ½ŠĶ£Õū¶Ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ·½·Ø | æĘѧŌĄķ |
| A | ÓĆĻ“µÓ¼ĮĒåĻ“ÓĶĪŪ | ĄūÓĆĮĖĻ“µÓ¼ĮµÄČé»Æ×÷ÓĆ |
| B | ÓƵŖĘų×÷Ģī³äµĘÅŻŃÓ³¤µĘÅŻŹŁĆü | µŖĘų»ÆѧŠŌÖŹ½ĻĪČ¶Ø |
| C | ¹ųøĒøĒĆš×Å»šµÄÓĶ¹ų | ½µµĶĪĀ¶Čµ½æÉČ¼Īļ×Å»šµćŅŌĻĀ |
| D | ŠāŹ“µÄĖųŠ¾ÖŠ¼ÓÉŁĮæĒ¦±ŹŠ¾Š¼ | ŹÆÄ«ÓŠČó»¬×÷ÓĆ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
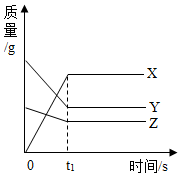 ČēĶ¼±ķŹ¾Ä³øö»Æѧ·“Ó¦¹ż³ĢÖŠø÷ĪļÖŹÖŹĮæÓėŹ±¼äµÄ¹ŲĻµ£¬ĻĀĮŠĆčŹöÕżČ·µÄŹĒ£Ø””””£©
ČēĶ¼±ķŹ¾Ä³øö»Æѧ·“Ó¦¹ż³ĢÖŠø÷ĪļÖŹÖŹĮæÓėŹ±¼äµÄ¹ŲĻµ£¬ĻĀĮŠĆčŹöÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆ·“Ó¦ŹĒ·Ö½ā·“Ó¦ | |
| B£® | XŹĒ·“Ó¦Īļ£¬YŗĶZŹĒÉś³ÉĪļ | |
| C£® | t1Ź±æĢ£¬·“Ó¦ĪļĶźČ«ĻūŗÄĶź | |
| D£® | t1Ź±æĢ£¬XµÄÖŹĮæµČÓŚYŗĶZ¼õÉŁµÄÖŹĮæÖ®ŗĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com