
分析 (1)根据酸碱指示剂在酸碱盐中的显色进行分析;
根据滴加盐酸的量利用方程式中的比例关系进行分析;
根据氯化钠的溶解度受温度的影响进行分析;
(2)根据氢氧化钠极易和空气中的二氧化碳反应进行分析;
(3)根据氢氧化钠和盐酸发生中和反应后溶液中是否存在盐酸进行判断.
解答 解:
(1)酚酞遇到碱性溶液变红色,遇到酸性和中性的液体不变色,滴加盐酸后只要酚酞由红色变成无色,就证明没有氢氧化钠了,两者发生了反应,
设反应后生成氯化钠的质量为x,
NaOH+HCl=NaCl+H2O
36.5 58.5
100g×3.65% x
$\frac{36.5}{100g×3.65%}=\frac{58.5}{x}$
x=5.85g
反应后的溶液质量是:100g+100g=200g,
所以反应后的溶质质量分数为$\frac{5.85g}{200g}×$100%≈2.1%
氯化钠的溶解度受温度影响变化较小,所以可以蒸发溶剂使晶体析出,
故答案为:无色,2.1%,蒸发溶剂;
(2)蘸取的氢氧化钠和空气中的二氧化碳会生成碳酸钠,所以蘸取之前,需要清洗,防止影响实验效果,故答案为:洗涤擦拭;
(3)先向稀硫酸中逐滴加入氢氧化钠溶液,再滴入碳酸钠溶液,实验过程中无气泡逸出,说明加入氢氧化钠溶液可以与稀硫酸反应;
加入碳酸钠溶液时有气泡逸出,说明溶液中稀硫酸,因此,该实验不能证明稀硫酸与氢氧化钠溶液发生了中和反应.盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
要证明稀硫酸与氢氧化钠溶液发生了中和反应,需补充如下实验:向2mL稀硫酸中直接滴加碳酸钠溶液至无气泡产生,记录消耗碳酸钠溶液的体积,若此体积大于乙的实验中消耗的碳酸钠溶液的体积,则证明在乙的实验中稀硫酸与氢氧化钠溶液发生了中和反应,所以本题答案为:逐滴加入碳酸钠溶液至无气泡产生,记录消耗的碳酸钠溶液的体积为V3 mL,V3 mL>V2mL,证明在乙的实验中稀硫酸与氢氧化钠溶液发生了中和反应;
根据酸碱的性质可知,氢氧化铝、铁锈、锌粒都能与酸反应,氯化钠不反应,故选C
答案:
(1)无色,2.1%,蒸发溶剂
(2)洗涤擦拭
(3)Na2CO3+2HCl═2NaCl+H2O+CO2↑ 甲 逐滴加入碳酸钠溶液至无气泡产生,记录消耗的碳酸钠溶液的体积为V3 mL,V3 mL>V2mL,证明在乙的实验中稀硫酸与氢氧化钠溶液发生了中和反应; C
点评 此题在以往对中和反应探究考查的基础上又有所拓展,从定量研究的角度对同学们提出了要求.很多同学由于基础知识掌握不牢固,心理素质较差,缺乏分析推理和实验探究能力而不能顺利解答此类综合性问题.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | +3 | B. | +2 | C. | 0 | D. | -1 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用食盐除去热水瓶内胆壁上的水垢 | |
| B. | 用食品级的小苏打和柠檬酸等可自制汽水 | |
| C. | 制作简易净水器时,为了达到更好的净水效果,活性炭应该放在最上层 | |
| D. | 用加热的方法修补电木等热固性塑料 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中的CO | 在空气中点燃 |
| B | 区分羊毛与合成纤维 | 点燃,闻气味 |
| C | 分离铁粉和铜粉混合物 | 加入足量稀硫酸,过滤 |
| D | 区分NaOH和Ca(OH)2溶液 | 分别加入碳酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
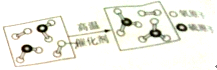 某反应的微观示意图如图所示.请分析下列说法正确的是( )
某反应的微观示意图如图所示.请分析下列说法正确的是( )| A. | 反应前的物质都是化合物 | |
| B. | 反应后的物质是氧气和二氧化碳的混合物 | |
| C. | 整个反应是2种物质反应生成另外2种物质 | |
| D. | 整个实验过程中,该反应化学方程式为2SO2+O2$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$2SO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com