
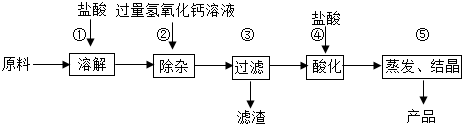
分析 (1)根据所学知识可以知道碳酸钙可以和盐酸反应生成氯化钙,氧化铁和盐酸反应生成氯化铁来分析;
(2)在工业碳酸钙中含有氧化铁,所以加入盐酸后,氧化铁可以和盐酸反应生成了氯化铁,进而和氢氧化钙反应,可以据此写出该反应的化学方程式;
(3)由于一开始加入的氢氧化钙是过量的,如果直接蒸发则会使制得的氯化钙不纯,同时要知道盐酸具有挥发性,可以据此答题.
解答 解:(1)碳酸钙可以和盐酸反应生成氯化钙,氧化铁和盐酸反应生成氯化铁;可判断盐酸与原料中的物质反应生成的两种氯化物是氯化钙和氯化铁;
(2)在工业碳酸钙中含有氧化铁,所以加入盐酸后,氧化铁可以和盐酸反应生成了氯化铁,氯化铁和加入的氢氧化钙反应生成了氢氧化铁,故可以写出该反应的化学方程式:3Ca(OH)2 +2FeCl3 ═3CaCl2 +2Fe(OH)3↓;
(3)由于加入的氢氧化钙是过量的,所以在最后的滤液中含有氢氧化钙,如果直接蒸发则会使制得的氯化钙不纯,所以加入稀盐酸来中和氢氧化钙,而盐酸具有挥发性,所以加热时盐酸挥发出来,剩余的固体为氯化钙.
故答案为:(1)CaCl2;FeCl3;
(2)3Ca(OH)2+2FeCl3=3CaCl2+2Fe(OH)3↓;
(3)过量的氢氧化钙;挥发.
点评 熟练掌握常见物质的化学性质,解答时要仔细分析生产流程图,明确流程图中各操作在生产过程中的作用,整体把握生产过程,这是解答所提出的问题的基础.


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:初中化学 来源: 题型:选择题
| A. | 用清洁能源代替化石燃料 | B. | 将生活垃圾焚烧处理 | ||
| C. | 大力发展煤炭火力发电 | D. | 多开私家车出行 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
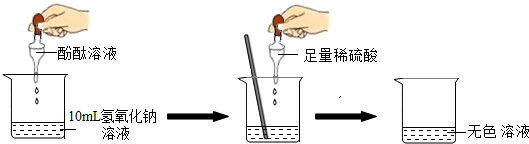
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
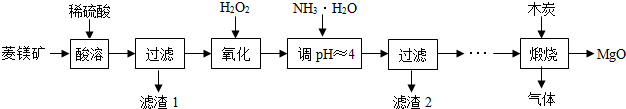
| 氢氧化物 | Fe(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 8.6 |
| 完全沉淀的pH | 3.2 | 11.1 |

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 炒菜时油锅着火,立即盖上锅盖 | |
| B. | 高层住房着火时,立即打开所有门窗 | |
| C. | 厨房燃气管漏气,立即关闭阀门开窗通风 | |
| D. | 扑灭图书档案发生的火灾时最适宜用液态二氧化碳灭火器 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质种类 | 葡萄汗 | 苹果汁 | 牛奶 | 鸡蛋清 |
| pH | 3.5~4.5 | 2.9~3.3 | 6.3~6.6 | 7.6~8.0 |
| A. | 苹果汁和葡萄汁都显酸性 | |
| B. | 苹果汁比葡萄汁的酸性强 | |
| C. | 鸡蛋清和牛奶都显碱性 | |
| D. | 胃酸过多的人不宜多喝葡萄汁和苹果汁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com