
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源:2017届广东省汕头市金平区九年级教学质量监测化学试卷(解析版) 题型:选择填充题
中国丝绸有几千年的历史传承,古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是
A. 草木灰 B. 食醋 C. 烧碱 D. 生石灰
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 磷在空气中燃烧,有大量白雾生成 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 木炭在空气中燃烧,发出白光 | |
| D. | 铁丝在氧气中燃烧,生成一种黑色的固体四氧化三铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 通过闻气味的方法可以鉴别酱油与食醋 | |
| B. | 利用C、CO、H2的还原性来冶炼金属 | |
| C. | 推广使用可降解的塑料制品 | |
| D. | 在猪饲料中添加瘦肉精以满足人们对瘦猪肉的需求 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化工厂用氨、二氧化碳和水制碳酸氢铵:NH3+H2O+CO2=NH4HCO3 | |
| B. | 实验室用石灰石和稀盐酸反应制取二氧化碳:CaCO3+2HCl=CaCl2+CO2↑+H2O | |
| C. | 氯化铵与消石灰混合研磨产生氨气:2NH4C1+Ca(OH)2=CaCl2+2NH3↑+2H2O | |
| D. | 氢化钙(CaH2)与水反应可以得到氢气:CaH2+2H2O=Ca(OH)2+2H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
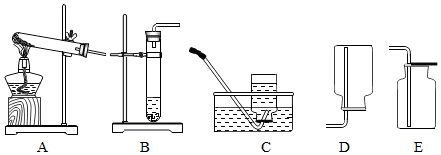
| 装置A | 装置B | |
| 反应状态 | 固体反应生成气体 | 固体和液体反应生成气体 |
| 反应条件 | 加热 | 无需加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com