
���� ��1����̪������ɫ�������ɫ�����ݷ�̪��ɫ�ı仯ȷ����Һ���е������
��2��������������������ķ�Ӧ��ָʾ���ı�ɫ�����ش�
��3�����ݻ�ѧ����ʽ���������Ƶ������ɼ�����ȥϡ���������������
��� �⣺��1����̪������ָʾ����Եģ����ݷ�̪��ɫ�ı仯�������ж��кͷ�Ӧ���е������
��2�������ɫ��ʧ˲������μ�ϡ���ᣬ��Һ�����ԣ������ɫ����ʱ��Һ�е����������ɵ��Ȼ��ƺ�ʣ���ϡ���ᣬ���ʵĻ�ѧʽ�ǣ�NaCl��HCl��
��3������ȥϡ�������������Ϊx
NaOH+HCl=NaCl+H2O
40 36.5
10g��8% x
$\frac{40}{36.5}=\frac{10g��8%}{x}$ ��ã�x=0.73g
����ȥϡ����������ǣ�$\frac{0.73g}{10%}$=7.3g
�ʴ�Ϊ�����жϷ�Ӧ���кͽ��еij̶ȣ����ޣ�NaCl��HCl���۹���ȥϡ�����������7.3g��
���� ������Ҫ�Ӷ����ĽǶȶ��кͷ�Ӧ�������о���Ҫ���ջ�ѧ����ʽ�ļ��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
| �����Ȼ�����Һ���� | ��һ�� | �ڶ��� | ������ |
| ���ɳ�����������/g | 4 | m | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ع�������ˮ�ɵõ��Ϻ�ɫ��Һ | |
| B�� | ���ȵ�ľ̿��������ȼ��ʱ�������� | |
| C�� | ϸ��˿����ʢ�������ļ���ƿ�о���ȼ�� | |
| D�� | ���̪��Һ����μ��백ˮ��Һ����ɫ����ɫ��ɺ�ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
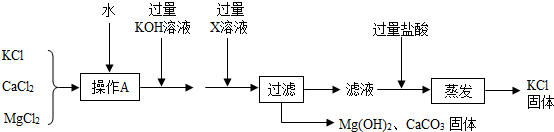
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
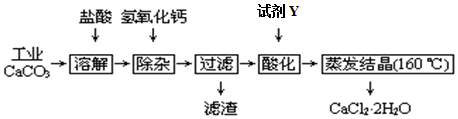
| �������� | Fe��OH��3 | Al��OH��3 | |
| ��ʼ����ʱ��pH | 2.3 | 4.0 | ��ʼ�ܽ⣺7.8 |
| ��ȫ����ʱ��pH | 3.7 | 5.2 | ��ȫ�ܽ⣺10.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
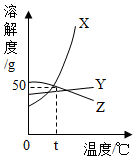 ��ͼ��X��Y��Z�������ʵ��ܽ�����ߣ�����˵����ȷ���ǣ�������
��ͼ��X��Y��Z�������ʵ��ܽ�����ߣ�����˵����ȷ���ǣ�������| A�� | �ܽ�ȱ仯���¶�Ӱ��������Y | |
| B�� | t��ʱ������Z��Һ��������������Ϊ50% | |
| C�� | Ҫ���X��Y�Ļ����Һ�з��������X������ȴ�ȱ�����Һ | |
| D�� | t��ʱ��Ҫ�뽵���������ʱ�����Һ�����������������ɲ��������ܼ��������¶ȵķ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȼ��ú̿���� | B�� | ��չ�����Դ | C�� | �ֵ���ˮ���� | D�� | ѡ����ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij��ȤС���ڽ��С�����������ȼ�ա���ʵ��ʱ���ֲ�����SO2���д̼�����ζ���������ϵ�֪���������нϴ�Σ�������ֱ���ŷŵ������л���Ⱦ�������������ǶԸ�ʵ����ж�Ľ�����ͼ��ʾ��
ij��ȤС���ڽ��С�����������ȼ�ա���ʵ��ʱ���ֲ�����SO2���д̼�����ζ���������ϵ�֪���������нϴ�Σ�������ֱ���ŷŵ������л���Ⱦ�������������ǶԸ�ʵ����ж�Ľ�����ͼ��ʾ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com