
 请按如图所示的硫酸知识网络填空(图中“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质):
请按如图所示的硫酸知识网络填空(图中“-”表示相连的两种物质能发生反应,“→”表示一种物质能转化成另一种物质):

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:初中化学 来源: 题型:


查看答案和解析>>
科目:初中化学 来源: 题型:解答题


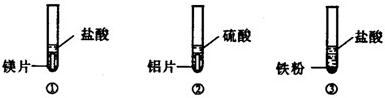
| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出,反应到5分钟时,铝片上还在冒气泡 | 铁粉中不断有无色气泡冒出,气泡量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
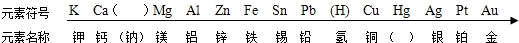
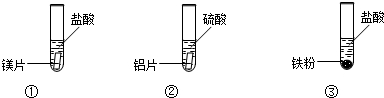
| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出,反应到5分钟时,铝片上还在冒气泡 | 铁粉中不断有无色气泡冒出,气泡量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
查看答案和解析>>
科目:初中化学 来源:2012-2013学年浙江省八里店二中九年级(下)期中化学试卷(解析版) 题型:填空题
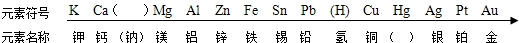

| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出,反应到5分钟时,铝片上还在冒气泡 | 铁粉中不断有无色气泡冒出,气泡量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
查看答案和解析>>
科目:初中化学 来源:2009-2010学年福建省福州三中金山校区九年级(上)期末化学复习试卷(2)(解析版) 题型:填空题
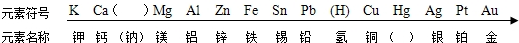
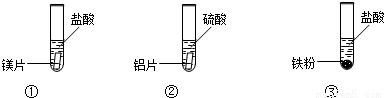
| 编号 | ① | ② | ③ |
| 现象 | 金属表面立即有大量无色气泡冒出,反应不到5分钟金属已消失 | 金属表面慢慢有少量无色气泡冒出,反应到5分钟时,铝片上还在冒气泡 | 铁粉中不断有无色气泡冒出,气泡量比②中多,溶液逐渐显浅绿色,反应到5分钟时,铁粉还在冒气泡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com