
【题目】在探究金属的活动性顺序时,某同学将一定质量的Zn粉放入AgNO3与Cu(NO3)2的混合溶液中,实验流程如图所示,请分析回答:
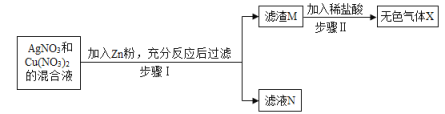
(1)步骤Ⅱ中生成的无色气体X是_____,该反应的基本反应类型是_____.
(2)滤液N中的溶质是_____;生成该溶质的化学方程式_____________。
【答案】氢气 置换反应 硝酸锌 Zn+2AgNO3═Zn(NO3)2+2Ag、Zn+Cu(NO3)2═Zn(NO3)2+Cu
【解析】
由于金属的活动性是:锌>铜>银,将一定质量的Zn粉放入AgNO3与Cu(NO3)2的混合溶液中,锌先与硝酸银反应生成了银和硝酸锌,当硝酸银完全反应后,再与硝酸铜反应生成了硝酸锌和铜。由流程图可知,向过滤后的滤渣中加稀硫酸有气泡生成,说明了锌粉是过量的,生成的无色气体应为氢气,溶液中的硝酸银和硝酸铜完全发生了反应,所以:
(1)步骤Ⅱ中生成的无色气体X是氢气,该反应锌与稀硫酸反应生成了硫酸锌和氢气,基本反应类型是由一种单质和一种化合物生成另一种单质和另一种化合物的置换反应;
(2)因硝酸铜和硝酸银完全反应,滤液N中的溶质只有生成的硝酸锌;所发生的反应的化学方程式有:Zn+2AgNO3═Zn(NO3)2+2Ag、Zn+Cu(NO3)2═Zn(NO3)2+Cu。


 高中必刷题系列答案
高中必刷题系列答案科目:初中化学 来源: 题型:
【题目】利用如图装置研究二氧化碳的性质。
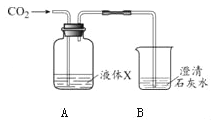
(1)若X为紫色石蕊溶液,观察到的现象是_____、澄清石灰水变浑浊。B中发生反应的化学方程式为_____。
(2)若X为氢氧化钠溶液,通入与(1)中等体积的CO2,观察到B中无明显现象,其原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲和乙两种固态物质的饱和溶液中溶质质量分数与温度的关系如图8所示。下列说法不正确的是

A. 甲和乙两种物质的溶解度随温度的升高而增大
B. t1℃时,甲和乙两种物质的溶解度相等
C. t1℃时,甲和乙两种物质溶液的溶质质量分数相等
D. 25g乙物质完全溶于100g水中所需的最低温度是t2℃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)“微观—宏观—符号”三重表征是化学独特的表示物质及其变化的方法。请结合图示完成下列问题:
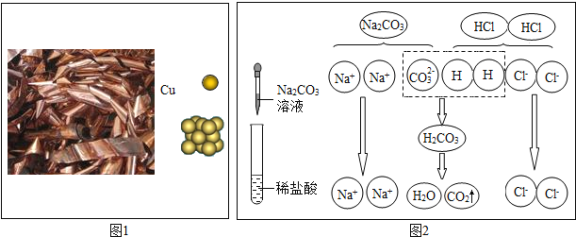
(1)图1中,“Ca”表示多种信息,如表示铜元素、金属铜单质,还能表示 ;
(2)从微粒的角度说明图2反应的实质是 ;
(3)为减少温室气体排放,人们积极寻找不含碳元素的燃料。经研究发现NH3燃烧的产物没有污染,且释放大量能量,有一定应用前景。其反应的微观示意图如图3所示:
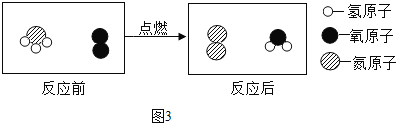
该反应的化学方程式为 ,其基本反应类型属于 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组利用下列装置进行气体的制取实验,请分析回答下列问题。
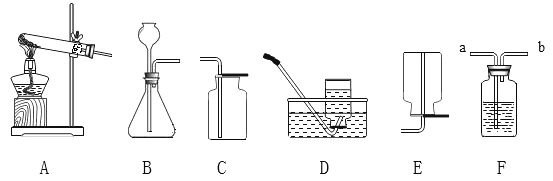
(1)选用A装置制取氧气的化学方程式_____;若要收集干燥的氧气,应使用装置_____进行收集(填选项字母)
(2)A、D连接,制取的氧气不纯的原因是_____________(写一点即可);
(3)实验室制取二氧化碳选择的发生装置和收集装置是_____(填选项字母),选择该发生装置的依据是_____,检验二氧化碳是否收集满的方法是_________________;
(4)将二氧化碳通入盛有紫色石蕊溶液的F装置中;观察到的现象是_________;化学方程式__________________。
(5)若用F装置检验制得的气体是否为二氧化碳,气体应从_______ 口通入(填“a”或“b”);F装置内发生反应的化学方程式_______________。
(6)实验室可用加热氯化铵和氢氧化钙的固体混合物来制取NH3,则实验室制取NH3的发生装置为_______(填选项字母);NO气体难溶于水且易与氧气发生反应,则实验室收集NO气体应选择的装置是_______(填选项字母)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组同学在协助老师整理化学试剂时,发现一瓶标签残缺的无色液体(如图)(温馨提示:标签上的5%表示该混合物中主要成分所占的质量分数)。他们对此瓶无色液体是什么产生了兴趣,于是进行了如下探究。
![]()
(大胆猜想)猜想一:水 猜想二:稀硫酸 猜想三:过氧化氢溶液
小组同学对标签又进行了仔细的观察、分析,他们一致认为猜想一不合理。理由是_____。
(设计方案)同学们结合所学知识设计出如下探究方案:向盛有少量二氧化锰的试管中加入适量的该液体,并将带火星的木条放在试管口。
(实验与事实)按上述方案进行实验,发现有大量气泡产生,带火星的木条复燃。
(结论与解释)
(1)以上事实证明猜想_____是正确的;
(2)产生气体的反应可用化学方程式表示为_____。
(反思与评价)(1)为避免在今后的实验中出现标签残缺的情况,在倾倒液体时应注意_____。
(拓展与迁移)根据探究结果,重新贴好标签。标签上化学式中氧元素的合价为_____价(已知氢元素显+1价)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸亚铁(FeCO3)是生产补血剂的原料。以下是某同学设计的利用铁矿烧渣(主要成分为Fe2O3、FeO和泥沙等)制取碳酸亚铁的实验流程图:
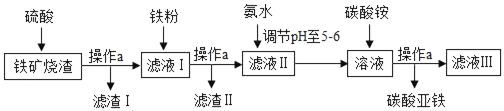
请回答下列问题:
(1)操作a中需要用到的玻璃仪器主要有烧杯、玻璃棒和_____。
(2)加入过量稀硫酸前要将铁矿烧渣粉碎的目的是_____滤液I中含有的溶质是:FeSO4、_____(填化学式)。
(3)滤液Ⅰ中加入铁粉后可能发生的化学方程式:
①Fe+Fe2(SO4)3=3FeSO4
②_____。
(4)加入碳酸铵得到碳酸亚铁的反应化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面短文,回答相关问题。
酒是餐桌上常见的一种饮品,男女老幼均有饮用者,然而,酒后窘态百出,既有呕吐不止的,又有精神亢奋的;既有自己被送往医院的,又有酒驾造成交通事故的,因此,提倡“饮酒要适量,酒后不开车”,是对自己和他人负责的良好行为。
白酒、红酒、啤酒等酒类,都含有酒精,其化学名称是乙醇(C2H5OH),酒精进入体内,很容易通过胃肠黏膜进入血液当中,酒精在人体内的代谢过程95%是靠肝脏分解的,分解过程如“图1”所示。酒精分解经历两个过程,①乙醇→乙醛的过程,需要肝脏中的乙醇脱氢酶参与,若摄入酒精量过大,分解相对比较慢。乙醇聚集体内,会刺激胃黏膜,出现胃部不适,酒精也会抑制神经系统,导致睡眠紊乱。②乙醛→乙酸的过程,需要肝脏中的乙醛脱氢酶参与,不同的人体内的乙醛脱氢酶含量差别很大,乙醛聚集导致脸部发红,搏动性头痛、心慌、恶心等症状。另外,以上两个转化过程,都要消耗大量的能量,导致酒精性低血糖,出现出汗、饥饿、心慌、颤抖、面色苍白等症状。
在肝脏内没有完全分解的酒精和乙醛,会通过血液,由心脏送往全身。根据科学家的研究,当血液中酒精的浓度达到0.05%时,人就会出现“酒意”,开始进入兴奋状态;酒精的浓度达到 0.1%时,人会变得性情豪迈、动作夸张,达到 0.2%时,便进入了酩酊时期,人会步履蹒跚、呼吸急促、恶心呕吐;超过0.3%,人便步行困难、言语不清、烂醉如泥;一旦超过0.4%,饮酒者就昏睡不醒了。
|
|
图1﹣肝脏分解乙醇的过程 | 图2﹣饮酒前后指标对比 |
为了研究乙醇对人体神经行为能力的影响,科研人员选取若干自愿者、等量饮用同一种酒。参照世卫组织神经行为能力测试标准,测试简单反应时(对简单信号作出反应的最短时间)、视觉保留(对视觉信号记忆的准确数)和血液中乙醇浓度。以受试者自身未饮酒时为对照,计算能力指数相对值,结果如“图2”所示。
车辆驾驶人员血液中的酒精含量大于或者等于20mg/100mL,小于80mg/100mL属于饮酒后驾车;血液中的酒精含量大于或者等于80mg/100mL为醉酒驾车。
青少年为了自己的身体健康,要远离酒类;为了家庭幸福,要劝告父母饮酒适量,禁止酒后驾车。
(1)乙醇的俗称是_____。
(2)酒后导致脸红的主要物质_____。
A 乙醇 B 乙醛 C 乙酸
(3)乙酸俗称为醋酸,它能使紫色石蕊溶液变为_____。
(4)人体血液中乙醇的浓度最高点是在饮酒后_____小时。
A 0.5 B 1.5 C 3.5
(5)下列说法正确的是_____。
A 肝脏能够把进入人体内的酒精全部分解
B 乙醇中碳元素的质量分数最大
C 当人体血液中乙醇浓度最大时,简单反应时和视觉保留最差
D 血液中的酒精含量只要达到80mg/100mL就会定为醉酒驾车
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】微观示意图可以帮助我们更好地认识化学反应的宏观事实。根据如图回答:
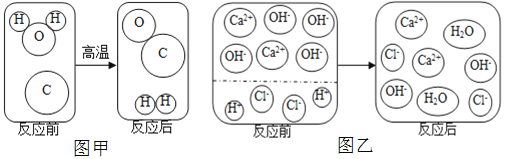
(1)图甲表示的是生产水煤气的微观示意图,该反应的化学方程式为___________,该反应类型属于_________ (基本反应类型)。
(2)图乙表示的是向滴有紫色石蕊的稀盐酸中加入氢氧化钙溶液,当溶液pH逐渐变为7时,该过程看到的实验现象为____________。
(3)从图乙反应后的微观示意图分析可知溶液颜色最终呈_________________。
(4)图乙反应的微观本质是___________________________________ (用文字描述)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com