
分析 根据质量守恒定律和反应只生成二氧化碳气体可求二氧化碳的质量,进而根据化学方程式求算HCl和碳酸钙的质量,最后求算对应的质量分数.
解答 解:根据质量守恒定律可知,生成的二氧化碳的质量为25g+200g-216.2g=8.8g
设反应掉的HCl的质量为x,碳酸钙的质量为y.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
y x 8.8g
$\frac{100}{y}$=$\frac{73}{x}$=$\frac{44}{8.8g}$
x=14.6g
y=20g
所用稀盐酸的溶质的质量分数为$\frac{14.6g}{200g}$×100%=7.3%
石灰石中碳酸钙的质量分数为$\frac{20g}{25g}$×100%=80%.
答:(1)生成二氧化碳的质量是 8.8g;
(2)所用稀盐酸的溶质质量分数是7.3%;
(3)石灰石中碳酸钙的质量分数是80%.
点评 首先确定计算所需要用的数据,也就是数据的有效性,其次确定多少未知数待求,所有根据一个化学方程式计算的数据力争一次性全部求算完毕.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | O2和O3都是单质 | B. | O2和O3都是同一种物质 | ||
| C. | O2和O3的性质完全相同 | D. | 该反应是物理变化而不是化学变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| B. | 切完西瓜的菜刀洗净擦干放在通风干燥处可以防止生锈 | |
| C. | 用黄铜片(铜锌合金)和铜片相互刻画,黄铜片上留有划痕 | |
| D. | 将二氧化碳通入燃着的两支高低蜡烛的烧杯中,蜡烛自低到高依次熄灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
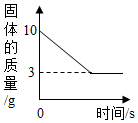 某同学取Fe粉与Cu粉混合物样品,加入足量的稀盐酸,待反应完全后过滤,称得固体质量如图所示,试计算:
某同学取Fe粉与Cu粉混合物样品,加入足量的稀盐酸,待反应完全后过滤,称得固体质量如图所示,试计算:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
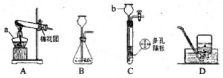 结合图示实验装置,回答下列问题.
结合图示实验装置,回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 盐酸的浓度(均取20mL) | 温度/℃ | 收集40mL气体所需时间/s |
| ① | 5% | 30 | 48 |
| ② | 10% | 20 | 41 |
| ③ | 5% | 20 | 69 |
| ④ | 10% | 30 | 32 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 如图为用红磷探究质量守恒定律的实验装置图.请完成下列探究过程:
如图为用红磷探究质量守恒定律的实验装置图.请完成下列探究过程:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图为A、B、C三种固体物质的溶解度曲线.下列有关说法正确的是( )
如图为A、B、C三种固体物质的溶解度曲线.下列有关说法正确的是( )| A. | A的溶解度大于B | |
| B. | t2℃时,A、B溶液的溶质质量分数都是b% | |
| C. | B可能是氯化钠,可用蒸发溶剂的方法从溶液中析出晶体 | |
| D. | 将等质量的A、B、C三种物质的饱和溶液都从t1℃升温到 t2℃,A、B溶液的溶质质量分数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com