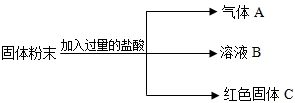
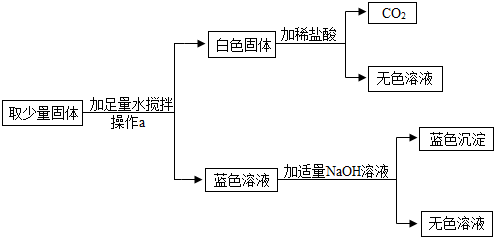
有一包固体粉末,可能含有氯化钠、碳酸钙、硝酸钾、硝酸银中的一种或几种.取少量该固体粉末加到足量的水中,充分振荡,得到白色沉淀,向该白色沉淀中加入稀盐酸,只有部分溶解,且有气体放出.
请你回答:
(1)该固体粉末中一定含有 ;
(2)写出实验过程中发生反应的化学方程式:
① ;
② ;基本反应类型是 .
【答案】分析:根据物质的性质进行分析,取少量该固体粉末加到足量的水中,充分振荡,得到白色沉淀,则沉淀可能为碳酸钙、氯化银,向该白色沉淀中加入稀盐酸,只有部分溶解,且有气体放出,则一定含有碳酸钙和氯化银沉淀,要生成氯化银,原粉末中含有氯化钠和硝酸银.
解答:解:取少量该固体粉末加到足量的水中,充分振荡,得到白色沉淀,则沉淀可能为碳酸钙、氯化银,向该白色沉淀中加入稀盐酸,只有部分溶解,且有气体放出,则一定含有碳酸钙和氯化银沉淀,要生成氯化银,原粉末中含有氯化钠和硝酸银;
(1)该固体粉末中一定含有 NaCl、AgNO3、CaCO3,故填:NaCl、AgNO3、CaCO3;
(2)氯化钠能与硝酸银反应生成氯化银沉淀和硝酸钠,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,属于复分解反应,故填:NaCl+AgNO3═AgCl↓+NaNO3,CaCO3+2HCl═CaCl2++CO2↑+H2O,复分解反应.
点评:本题为常见物质组成推断题,完成此题,可以依据题干提供的信息结合物质的性质进行.



 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案