
(1)CuSO4+2NaOH===Cu(OH)2↓ +Na2SO4,该反应的基本类型是——反应。
(2)亚硝酸钠是一种工业用盐,外观与食盐相似,误食会引起中毒,其水溶液pH大于7。鉴别亚硝酸钠和食盐两种无色溶液可选用的试剂是——。
(3)为了检验曝露在空气中的氢氧化钠溶液是否变质,可以选择酸、碱、盐三种不同物质类别的试剂进行检验。请各举一例写出它们的化学式:酸——、碱——、盐——。
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验序号 | 实验1 | 实验2 | 实验3 |
| 方 案 |  |  |  |
| 现 象 | A中铝片表面有红色固体析出;B中铝片无明显现象. | ② ② | 与A中的现象相同 |
| 结 论 | 溶液中对氧化膜产生了破坏作用的离子可能是 ① ① . | 除去表面氧化膜的铝片会与CuSO4溶液反应.该反应的化学方程式 ③ ③ . | 验证了实验1的结论. |
查看答案和解析>>
科目:初中化学 来源: 题型:
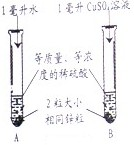 11、小明和同学用稀硫酸与锌制取氢气时,发现添加少量硫酸铜溶液能加快反应.硫酸铜溶液是稀硫硫酸和锌反应的催化剂吗?硫酸铜溶液量的多少会影响反应速率吗?
11、小明和同学用稀硫酸与锌制取氢气时,发现添加少量硫酸铜溶液能加快反应.硫酸铜溶液是稀硫硫酸和锌反应的催化剂吗?硫酸铜溶液量的多少会影响反应速率吗?| 试管 | A | B | C | D | E | F |
| CuSO4溶液/毫升 | 0 | 0.5 | 1 | 1.5 | 2 | 4 |
| 水/毫升 | 4 | 3.5 | 3 | V1 | V2 | 0 |
| 收集H2所用的时间/秒 | 348 | 246 | 190 | 165 | 230 | 360 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com