
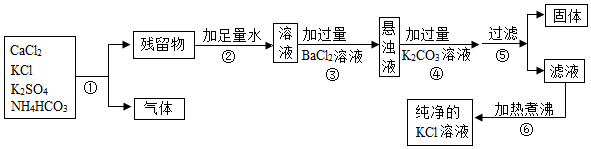
分析 (1)步骤①中除去碳酸氢铵的方法是加热,这是因为加热时碳酸氢铵分解生成氨气、水和二氧化碳;
(2)碳酸钾能和氯化钙反应生成碳酸钙沉淀和氯化钾,能和氯化钡反应生成白色沉淀碳酸钡和氯化钾;
(3)加入过量的碳酸钾溶液时,和氯化钙、氯化钡反应后剩余的碳酸钾没有除去,因此得到的氯化钾溶液中含有碳酸钾.
解答 解:(1)步骤①中除去碳酸氢铵的方法是加热,这是因为加热时碳酸氢铵分解生成氨气、水和二氧化碳,从而除去碳酸氢铵.
故填:加热.
(2)碳酸钾能和氯化钙反应生成碳酸钙沉淀和氯化钾,能和氯化钡反应生成白色沉淀碳酸钡和氯化钾,因此步骤④中加过量碳酸钾溶液的目的是除去氯化钙和过量的氯化钡.
故填:除去氯化钙和过量的氯化钡.
(3)此设计方案不严谨,这是因为加入过量的碳酸钾溶液时,和氯化钙、氯化钡反应后剩余的碳酸钾没有除去,因此得到的氯化钾溶液中含有碳酸钾.
故填:不严谨;反应后剩余的碳酸钾没有除去.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:选择题

| A. | 滤渣a的成分是碳酸钙和氢氧化镁 | |
| B. | 白色沉淀b的成份是碳酸钡 | |
| C. | 滤液中溶质的成分除氯化钠还有氢氧化钠、硫酸钠 | |
| D. | 若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则不能确定原样品中一定存在氯化镁 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金刚石、石墨充分燃烧的产物都是二氧化碳 | |
| B. | 金刚石和石墨的物理性质不同的原因是碳原子的排列方式不同 | |
| C. | 书写档案时规定使用碳素墨水,是因为常温下碳的化学性质不活泼 | |
| D. | 金刚石和石墨都是硬度最大的物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuSO4 NaOH KNO3 | B. | FeCl3 AgNO3 NaNO3 | ||
| C. | Na2CO3 HCl BaCl2 | D. | CaCl2 K2CO3 NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
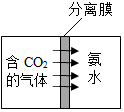 (1)二氧化硅可用于制造分离膜,利用“膜分离”技术可使二氧化碳穿过分离膜被氨水吸收(如图)生成可用作化肥的碳酸氢铵(NH4HCO3).
(1)二氧化硅可用于制造分离膜,利用“膜分离”技术可使二氧化碳穿过分离膜被氨水吸收(如图)生成可用作化肥的碳酸氢铵(NH4HCO3).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 粮食酿酒 | B. | 纺纱织布 | C. | 烧制瓷器 | D. | 冶炼生铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
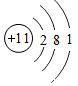 .钠元素位于元素周期表第三周期的开头(填“开头”、“中间”、“靠近尾部”或“结尾”)处.
.钠元素位于元素周期表第三周期的开头(填“开头”、“中间”、“靠近尾部”或“结尾”)处.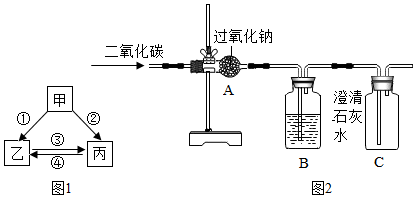
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com