
| A. | Ba(OH)2、Na2S04、K2C03 | B. | KOH,Na2C03,HC1 | ||
| C. | BaCl2、NaOH、H2S04 | D. | Ca(OH)2、H2SO4、NaOH |
分析 A、根据Ba(OH)2与K2CO3反应生成碳酸钡沉淀和氢氧化钾,Ba(OH)2与Na2S04溶液反应生成硫酸钡沉淀和氢氧化钠,溶液仍然呈碱性进行解答;
B、根据氢氧化钾和盐酸反应生成氯化钾和水以及碳酸钠和盐酸反应生成氯化钠、二氧化碳和水进行解答;
C、根据氯化钡和硫酸反应生成盐酸和硫酸钡进行解答;
D、根据Ca(OH)2、NaOH都与H2SO4发生中和反应进行解答.
解答 解:
A、Ba(OH)2与K2CO3反应生成碳酸钡沉淀和氢氧化钾,Ba(OH)2与Na2S04溶液反应生成硫酸钡沉淀和氢氧化钠,溶液仍然呈碱性,故正确;
B、氢氧化钾和盐酸反应生成氯化钾和水,碳酸钠和盐酸反应生成氯化钠、二氧化碳和水,所以当氢氧化钾或碳酸钠恰好反应时,溶液呈中性,氢氧化钾或碳酸钠有剩余时溶液呈碱性,故B不正确;
C、氯化钡和硫酸反应生成盐酸和硫酸钡,而NaOH与H2S04反应生成硫酸钾和水,盐酸与NaOH反应生成氯化钠与水,如果完全反应,溶液为中性;故C不正确;
D、Ca(OH)2、NaOH都与H2SO4发生中和反应,如果完全反应,溶液为中性,故D不正确.
故选:A.
点评 明确酸、碱的通性及酸、碱与常见物质之间的化学反应是解答本题的关键,学生需熟悉指示剂遇酸碱的变色情况来解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯酸钾不能分解 | B. | 有氧气产生但速度慢 | ||
| C. | 生成的氧气总量减少 | D. | 反应依然可在较低温度下进行 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 混合物 | 纯净物 | 氧化物 | 单质 |
| A | 石油 | 胆矾 | 四氧化三铁 | 水 |
| B | 天然气 | 纯净空气 | 二氧化碳 | 液氧 |
| C | 澄清石灰水 | 高锰酸钾 | 氧气 | 水银 |
| D | 水煤气 | 碳酸钠 | 冰水混合物 | 铁水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6g | 148.5g | 146.3g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
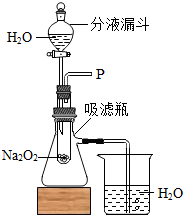 化学兴趣小组中某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小李很感兴趣,于是,他和同学们进行探究.
化学兴趣小组中某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小李很感兴趣,于是,他和同学们进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 (1)饲养观赏鱼,可以陶冶人的情操,增进人们对生活的热爱.空运观赏鱼,必须密封.为了解决鱼的吸氧问题,可在水中加入过氧化钙(化学式CaO2),过氧化钙与水反应生成的是氢氧化钙和氧气.写出过氧化钙与水反应的化学方程式2CaO2+2H2O═2Ca(OH)2+O2↑.
(1)饲养观赏鱼,可以陶冶人的情操,增进人们对生活的热爱.空运观赏鱼,必须密封.为了解决鱼的吸氧问题,可在水中加入过氧化钙(化学式CaO2),过氧化钙与水反应生成的是氢氧化钙和氧气.写出过氧化钙与水反应的化学方程式2CaO2+2H2O═2Ca(OH)2+O2↑.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com