
【题目】复分解反应存在这样一个规律:较强酸可制取较弱酸。中和反应、盐类的水解也是复分解反应,盐类的水解反应的逆反应是中和反应。盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解。
已知在常温下测得浓度均为0.lmol/L的下列6种溶液的pH:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 8.1 | 11.6 | 10.3 | 11.1 | 11.3 |
(1)请根据上述信息判断下列反应不能发生的是_____(填编号)。
A ![]()
B ![]()
C ![]()
D ![]()
E ![]()
F ![]()
(2)一些复分解反应的发生还遵循其他的规律、下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液
②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体
③蒸发KC1和NaNO3的混合溶液,首先析出NaCl晶体。
根据上述反应,总结出复分解反应发生的另一规律为_____。
(3)已知溶液的pH与氢离子浓度有直接关系。物质的量浓度均为0.05mol/L的下列五种物质的溶液中,pH由大到小的顺序是_____(填编号)。
①C6H5OH(苯酚) ②CH3COOH ③HClO4 ④HC1O ⑤H2SO4
(4)25℃时,M酸溶液的pH=a,N碱溶液的pH=b。若X为强酸,Y为强碱,且![]() ,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____。
,若两者等体积混合后,溶液的pH=7.此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是_____。
【答案】AD 反应能够由溶解度相对较大的物质向生成溶解度相对较小的物质方向进行 ①④②③⑤ 酸是二元强酸,碱是一元强碱
【解析】
(1)盐类的水解反应中,弱酸强碱盐中弱酸根离子对应的弱酸越弱,其盐越容易发生水解,故水解程度越大,pH越大,对应的弱酸酸性越弱。
A、pH:Na2CO3>NaClO>NaHCO3,说明对应的弱酸:酸性:H2CO3>HClO>HCO3-,较强酸可制取较弱酸,故碳酸与次氯酸钠反应应生成碳酸氢钠和次氯酸,即![]() ,符合题意;
,符合题意;
B、由A的分析可知,该反应能够发生,不符合题意;
C、pH:Na2CO3>C6H5ONa>NaHCO3,说明对应的弱酸,酸性:H2CO3>C6H5OH>HCO3-,较强酸可制取较弱酸,故碳酸与C6H5ONa反应生成C6H5OH和碳酸氢钠,反应可以发生,不符合题意;
D、由C的分析可知,该反应不能发生,符合题意;
E、pH:Na2CO3>C6H5ONa>NaHCO3,说明对应的弱酸,酸性:H2CO3>C6H5OH>HCO3-,较强酸可制取较弱酸,故碳酸钠与C6H5OH反应生成C6H5ONa和碳酸氢钠,符合题意;
F、pH:NaCN>CH3COONa,说明对应的弱酸,酸性:CH3COOH>HCN,较强酸可制取较弱酸,故CH3COOH与NaCN反应生成CH3COONa和HCN,反应可以发生,不符合题意。
故选AD;
(2)①石灰乳与碳酸钠反应生成碳酸钙和氢氧化钠,碳酸钙形成沉淀,说明该条件下,碳酸钠溶解度大于碳酸钙;
②碳酸氢铵与氯化钠生成氯化铵和碳酸氢钠,碳酸氢钠析出,说明,该条件下,碳酸氢铵溶解度大于碳酸氢钠;
③氯化钾与硝酸钠混合,氯化钠析出,氯化钠析出,说明该条件下,氯化钠溶解度小于氯化钾
由此可以看出,反应能够由溶解度相对较大的物质向生成溶解度相对较小的物质方向进行
(3)浓度均为0.05mol/L的六种物质的溶液,氢离子浓度越大pH越小,反之越大,强酸的电离程度大于弱酸的电离程度;pH:C6H5ONa>NaClO>CH3COONa,对应酸的酸性:CH3COOH>HClO>C6H5OH,硫酸和高氯酸属于强酸,硫酸是二元酸,故氢离子的浓度:硫酸>高氯酸,故pH由大到小的顺序是:①④②③⑤;
(4)M酸溶液的pH=a,N碱溶液的pH=b。若X为强酸,Y为强碱,且![]() ,若两者等体积混合后,溶液的pH=7,混合后,溶液显中性,说明c(H+)=c(OH-),若A为一元酸,B为一元碱,则酸的阴离子浓度等于碱的阳离子浓度,若酸是n元酸,碱是一元碱,则碱的阳离子浓度等于酸的阴离子浓度的n倍,则溶液中金属阳离子浓度大于酸根阴离子浓度,故此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是:酸是二元强酸,碱是一元强碱。
,若两者等体积混合后,溶液的pH=7,混合后,溶液显中性,说明c(H+)=c(OH-),若A为一元酸,B为一元碱,则酸的阴离子浓度等于碱的阳离子浓度,若酸是n元酸,碱是一元碱,则碱的阳离子浓度等于酸的阴离子浓度的n倍,则溶液中金属阳离子浓度大于酸根阴离子浓度,故此时溶液中金属阳离子浓度大于酸根阴离子浓度,其原因可能是:酸是二元强酸,碱是一元强碱。


 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:初中化学 来源: 题型:
【题目】如图是学生经常使用的交通工具——自行车,请完成下列各题:
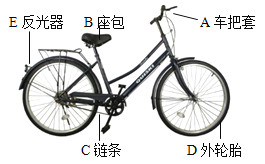
(1)自行车属于合成材料的是________ (选一种物质填序号)。
(2)车轮的钢圈在潮湿的空气中会生锈,生锈实质上是铁与空气中______发生 了一系列复杂的反应而造成的;
(3)利用铁生锈的原理在食品工业上还有应用。“纳米 Fe 粉”,可以用于食品保鲜,称之为“双吸剂”,请用 化学方法检验使用一段时间后的“双吸剂”是否完全失效,写出鉴别过程(填“操作、现象和结论”)_____________________
(4)用打气筒给轮胎打气后,轮胎内空气分子间的距离__________________ (填“大于”、“小于”、或“等于”)空气中分子之间的距离
(5)废旧的自行车不要随意丢弃,应回收利用,这样做的意义是__________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质a和b在一定条件下反应生成e和d的微观示意图如下:
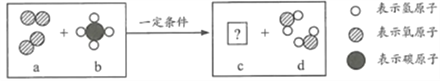
下列说法正确的是
A. 物质c是一氧化碳 B. 该反应不符合质量守恒定律
C. 该反应前后,原子的种类发生改变 D. 该反应前后,分子的个数保持不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图所示的实验,回答问题。
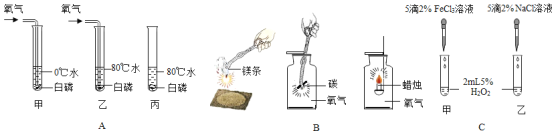
(1)A组实验中,通过对比__ 试管中的现象,可说明燃烧需要温度达到可燃物着火点。
(2)B组实验中,找出三个化学变化的一个共同点___。
(3)C组实验是探究哪种离子能促进H2O2分解的实验,现象是:甲中产生大量气泡,乙中可看到有极少量气泡出现,则加快H2O2分解的离子符号____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向 200.0g AgNO3 溶液中加入 m 克 Al 和 Cu 的混合粉末,搅拌,充分反应后过滤、洗涤、 干燥得到32.4g固体。向滤液中滴加稀盐酸,产生白色沉淀,下列说法正确的是
A.滤液的质量为 167.6g
B.混合粉末的质量可能为 8.0 克
C.过滤所得物体中加入稀盐酸可能会有气体生成
D.原 AgNO3 溶液的溶质质量分数为 25.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】推理是化学学习中常见的思维方法,下列推理正确的是
A.金刚石、石墨都是由碳原子构成的单质,它们的物理性质相同
B.某物质燃烧生成CO2和H2O,说明该物质中一定含有C、H两种元素
C.化学反应伴随着能量的变化,因此伴随能量变化的过程均为化学反应
D.复分解反应条件之一是有气体产生,因此有气体生成的反应均为复分解反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A—I是初中化学常见的九种物质。其中B为红色固体,E可作为干燥剂,I在溶液中是一种红褐色沉淀,它们相互转化的关系如图14所示(部分反应物、生成物及反应条件已略去)。

请回答下列问题:
(1)I物质的化学式为_______________。
(2)转化⑥的化学方程式为_______________________________________。
(3)反应④的基本反应类型为______________________。
(4)反应⑤在生产生活中的用途是_____________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】0.2%~0.5%的过氧乙酸(CH3COOOH)溶液是一种杀菌能力强的高效消毒剂。
(1)过氧乙酸分子中C、H、O原子的个数比为 ;
(2)过氧乙酸中 元素的质量分数最大;
(3)欲配制0.4%的过氧乙酸溶液1000g,需用20%的过氧乙酸溶液 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com