
| 实验步骤 | 实验现象 | 分析与结论 |
| ①在盛有少量蒸馏水的烧杯中滴入2~3滴石蕊试液 | 液体显紫色 | 结论:蒸馏水不能使酚酞变红 |
| ②在步骤①的烧杯中再滴加浓盐酸 | 试液变红 | 结论:酸性溶液能使紫色石蕊试液变红 |
| ③按图甲所示进行实验 | 烧杯B中试液变红 | 原因:由于浓盐酸具有较强的挥发性,所以倒扣的烧杯中会有大量的氯化氢分子存在,这些氯化氢的分子溶于烧杯B中会使该溶液变为稀盐酸而呈酸性,所以烧杯B中的紫色石蕊会变为红色, 结论:分子是不断运动的 |
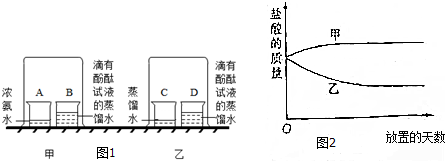
分析 (1)根据蒸馏水的溶液呈中性分析解答;根据稀盐酸的溶液呈酸性,能使石蕊变红分析解答即可;根据能盐酸容易会发出氯化氢分子的性质分析解答;
(2)①根据蒸馏水不能使酚酞变红,在第一个实验中已经可以证明了解答;
②根据浓盐酸具有挥发性,敞口放置时能使盐酸的质量变小解答;
③根据浓盐酸中溶剂所含氢原子数是溶质所含氢原子数的7倍可确定分子数的关系,然后利用相对分子质量来计算浓盐酸中溶质的质量分数.
解答 解:(1)①由于蒸馏水的溶液呈中性所以不能使石蕊变色,因此观察到的实验现象是烧杯里的水只能是紫色;
②在步骤①的烧杯中再滴加浓盐酸,稀盐酸溶液呈酸性,所以能使石蕊试液变红;
③由于浓盐酸具有较强的挥发性,所以倒扣的烧杯中会有大量的氯化氢分子存在,这些氯化氢的分子溶于烧杯B中会使该溶液变为稀盐酸而呈酸性,所以烧杯B中的紫色石蕊会变为红色,这也证明了构成物质的微粒的运动特点;
(2)①因为在第一个实验中已经可以证明蒸馏水不能使酚酞变红.故填:无必要;蒸馏水不能使酚酞变红,在第一个实验中已经可以证明了.
②浓盐酸具有挥发性,能挥发出溶质氯化氢,使溶液质量变小,观察图象,乙符合;
③盐酸的化学式是HCl,水的化学式为H2O,
由浓盐酸中溶剂所含氢原子数是溶质所含氢原子数的7倍可知,
氯化氢与水的分子数之比为2:7可满足题意,
设氯化氢分子2n个,则水分子7n个,
则该浓盐酸中溶质的质量分数为$\frac{2×36.5}{2×36.5+7×18}×$100%≈41.0%
答案:
(1)
| 实验步骤 | 实验现象 | 分析与结论 |
| ①在盛有少量蒸馏水的烧杯中滴入2~3滴石蕊试液 | 液体显紫色 | 结论: 蒸馏水不能使酚酞变红 |
| ②在步骤①的烧杯中再滴加浓盐酸 | 试液变红 | 结论: 酸性溶液能使紫色石蕊试液变红 |
| ③按图甲所示进行实验 | 烧杯B中试液变红 | 原因: 由于浓盐酸具有较强的挥发性,所以倒扣的烧杯中会有大量的氯化氢分子存在,这些氯化氢的分子溶于烧杯B中会使该溶液变为稀盐酸而呈酸性,所以烧杯B中的紫色石蕊会变为红色,结论: 分子是不断运动的 |
点评 此题借助实验探究,考查了分子运动的微观事实,解题时关键是利用相关的现象对所要解决的问题进行深入的分析.


科目:初中化学 来源: 题型:选择题
| A. | 溶液都是由一种溶质和一种溶剂组成的 | |
| B. | 溶液里各部分的性质是相同的 | |
| C. | 只要条件不变,糖水里的糖不会分离出来 | |
| D. | 通常不指明溶剂的溶液是水溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 事实 | 解释 |
| A | 10mL酒精和10mL水混合体积小于20mL | 分子之间有间隔 |
| B | 稀硫酸和稀盐酸化学性质相似也存在差异 | 溶液中都含有H+、也存在不同的SO42-、Cl-离子 |
| C | F Cl Cl F、Cl原子化学性质相似 | 化学反应中都易得到1个电子 |
| D | 蜡烛燃烧生成CO2和H2O | 蜡烛组成里含有碳、氢、氧元素 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验:
小乐发现切过咸菜的铁质菜刀很容易生锈,她猜测可能是咸菜中的盐水加快了铁的锈蚀,于是它设计了如图所示的实验:
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com