
【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验.
【提出问题】①氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰均匀混合加热
Ⅲ.将x g氯酸钾与1.0g氯化铜均匀混合加热
【实验现象分析】
Ⅲ中x的值应为 ,将实验Ⅰ和Ⅲ比较可证明 ,将实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和xg氯酸钾混合加热,现象与实验Ⅲ相同,此步骤是为了证明氧化铜在该化学反应前后 和 都不变.
【结论】氧化铜还能作氯酸钾分解的催化剂,请写出实验Ⅲ中的化学反应文字表达式
【实验反思】实验Ⅱ和Ⅲ对比是为了证明
【提出问题】②双氧水分解速度还和什么因素有关
【设计并完成实验】
双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生产生O2体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
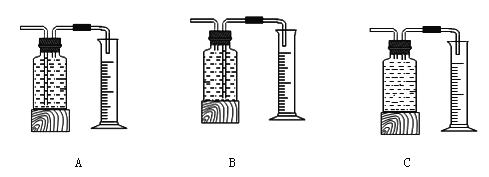
本实验中,测量O2体积的装置是 (填编号)
【结论】在相同条件下,双氧水的浓度越大,双氧水分解得越 。
【答案】【实验现象分析】3.0g;氧化铜能否改变氯酸钾分解的速率;质量;化学性质;【结论】氯酸钾![]() 氯化钾+氧气;【实验反思】氧化铜对氯酸钾的催化效果是否比二氧化锰更好;【设计并完成实验】C;快
氯化钾+氧气;【实验反思】氧化铜对氯酸钾的催化效果是否比二氧化锰更好;【设计并完成实验】C;快
【解析】试题分析:因为要探究催化剂形成对比试验,控制变量故【实验现象分析】Ⅲ中x的值应为3.0g, 将实验Ⅰ和Ⅲ比较可证明氧化铜能否改变氯酸钾分解的速率;实验Ⅲ反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和xg氯酸钾混合加热,现象与实验Ⅲ相同,此步骤是为了证明氧化铜在该化学反应前的质量和化学性质都不变;【结论】氧化铜还能作氯酸钾分解的催化剂,实验Ⅲ中的化学反应文字表达式为:氯酸钾![]() 氯化钾+氧气;【实验反思】实验Ⅱ和Ⅲ对比是为了证明氧化铜对氯酸钾的催化效果是否比二氧化锰更好;【提出问题】②双氧水分解速度还和什么因素有关【设计并完成实验】因为测定氧气的体积,就要把集气瓶中的水排出,用量同测量排出的水的体积,气体短进,液体才能压出,故选择C;【结论】在相同条件下,双氧水的浓度越大,双氧水分解得越快。
氯化钾+氧气;【实验反思】实验Ⅱ和Ⅲ对比是为了证明氧化铜对氯酸钾的催化效果是否比二氧化锰更好;【提出问题】②双氧水分解速度还和什么因素有关【设计并完成实验】因为测定氧气的体积,就要把集气瓶中的水排出,用量同测量排出的水的体积,气体短进,液体才能压出,故选择C;【结论】在相同条件下,双氧水的浓度越大,双氧水分解得越快。


科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是学习化学的基本方法。
(1)下列为A、B、C、D的原子或离子的结构示意图。
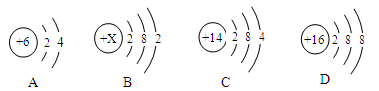
①B的原子结构示意图中X为_________;若D的元素符号为S,则D表示的微粒符号是_________。
②分析A、C的原子结构,你认为A与C具有相似化学性质的原因是__________________。
(2)下图为处理汽车尾气化学反应微观示意图,其中A、B、C、D表示4种物质,A和B在一定条件下反应可生成C 和D。
反应前 | 反应后 |
| ||
|
|
|
| |
③物质C中,各元素的质量比为_________。
④根据上述微观示意图,处理汽车尾气的化学反应方程式为_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“健康饮食、均衡营养”是青少年健康成长的重要保证。
①蛋白质是构成细胞的基本物质,是机体生长和修补受损组织的主要原料。处于生长发育期的青少年每天需要较多的蛋白质。下列物质中富含蛋白质的有 (填字母)。
 ②“食品安全”是一个永恒的话题。你认为下列认识不科学的是 (填字母)。
②“食品安全”是一个永恒的话题。你认为下列认识不科学的是 (填字母)。
A.任何食品都不可以使用食品添加剂
B.霉变的大米、花生,即使经过蒸煮也不能食用
C.含钙、锌的奶粉有利于补充人体所需的常量和微量元素
D.用亚硝酸钠代替食盐来腌渍食品
(2)“科技创新、材料发展”极大地促进了人类社会的进步。
①“辽宁号”航母的服役举世瞩目。钢铁是制造航母的主要材料,它易水与空气中的 等发生反应而锈蚀,请你列举一种防止钢铁锈蚀的方法 。
②可降解塑料的问世,既方便了生活,又减少了“白色污染”。塑料属于 材料(填“复合”或“合成”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】南京著名的风景点——珍珠泉,水底有大量的气泡冒出,像一串串珍珠,珍珠泉由此得名。某学生推测这种气体可能是沼气,查资料得知,沼气中含60%~70%的CH4,还含有CO2、N2和CO等。他想用实验检验珍珠泉冒出气体的组成,设计了如图甲所示的取气方法:

将空的雪碧汽水塑料瓶装满水,倒放在泉水中,瓶口对准水底冒出的气泡进行收集。
⑴这种集气方法叫 ,针对瓶口太小不便收集的缺点,在不换瓶的情况下,你改进的方法是 。
⑵如图乙所示,若用水将瓶中的气体排出,水龙头应接导管___________(填A或B)。
⑶假设将这种未知气体通过澄清石灰水,石灰水变浑浊,剩余气体通过浓硫酸(以上两步,能被吸收的气体均被完全吸收),再通入纯氧气中点燃,将燃烧后生成的气体依次通过无水硫酸铜(检验水)、澄清石灰水,观察到无水硫酸铜变蓝,石灰水变浑浊。仅由以上实验现象分析此未知气体的组成,结论是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)某城市住宅饮用水的处理过程如图所示:
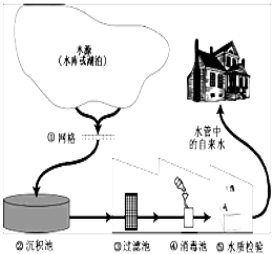
(1)步骤②所起的作用是__________(单选,填选项序号)。
A.杀死水中的细菌 B.减少水中氧气
C.使泥沙沉积至底部 D.分解有毒物质
(2)假如你是水质检验员,用简单的办法检验水样是不是硬水,可选用的试剂是_______________ ;若检验时发现水硬度高,你建议在饮用前可采取的常用处理办法是__________________。
(3)家庭净水器中含有大量的活性炭,活性炭起_________________作用。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知氯化镁样品中含有杂质氯化钠,某化学兴趣小组的同学通过以下实验测定其中氯化镁的质量分数:称取该样品15g溶于水得到溶液,然后将一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡(实验数据见下表)。
第1次 | 第2次 | 第3次 | 第4次 | |
加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
生成沉淀的质量/g | 2.9 | x | 8.7 | 8.7 |
(1)表中x = 。
(2)样品中氯化镁的质量分数是 。
(3)若实验室中只有80g质量分数为30%的氢氧化钠溶液,要想配成本实验所需溶质质量分数的氢氧化钠溶液,还需加入水的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(4分)下图为A、B两种固体物质的溶解度曲线。请根据图示回答:
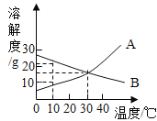
(1)A物质的溶解度随温度的升高而______________(填“增大”、“不变”或“减小”)。
(2)10℃时,A、B的溶解度大小关系是A_____________B(填“大于”、“等于”或“小于”)。
(3)将30℃的A、B两种接近饱和的溶液通过升高温度可达到饱和的是_________溶液。
(4)若将10℃的A、B两种饱和溶液的温度升高到30℃,此时两种溶液中溶质质量分数的大小关系是A_________B(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(11分)
下图A与B是实验室常用来制取气体的装置,根据所学知识回答以下问题:
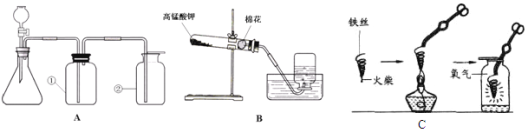
(1)装置A中②的仪器名称是 ,若想用装置A来制取的氧气,使用的药品是___________(填化学式);若想制取CO2,应选择装置_______(填“A”或“B”)。
(2)装置B表示正在用高锰酸钾制取氧气,其中还缺少的仪器是________,该反应的化学方程式为_____________________________________,实验完毕,为防止水倒吸,应________________________。
(3)装置A气密性的检验:先关闭分液漏斗活塞,然后加水浸没瓶②中导管的末端,用热毛巾捂住瓶①,若__________________________,则该装置漏气。
(4)图C中螺旋状铁丝的末端系一根火柴的作用是 。
(5)小明对铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录。请你分析回答:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | (未填) |
小明按图C实验时,上表中“未填”的实验现象是 ;
铁丝在氧气中燃烧为什么会火星四射?原因 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,请回答:

(1)当加入212g稀盐酸时,放出气体的质量为__________g
(2)碳酸钠样品中碳酸钠的质量分数为多少?(写出计算过程)
(3)加入106g稀盐酸(即A点)时烧杯中溶液溶质的质量分数为多少?(写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com