
在20℃时KCl的溶解度为34(g),现有20℃时KCl的饱和溶液100(g),若温度不变,蒸发掉10(g)水后溶液的质量变为
[ ]
A.90(g) B.86.6(g) C.59.7(g) D.无法确定
科目:初中化学 来源: 题型:阅读理解
| 影响固体物质的溶解能力 | 举例说明 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (1)在初中化学中,我们学习了溶液的有关知识.
(1)在初中化学中,我们学习了溶液的有关知识.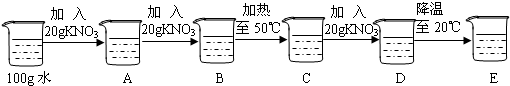
| 物质 | 与众不同的物质 | 理由 |
| KCl K2SO4 K2CO3 BaCO3 |
KCl | KCl中不含氧元素,其他物质中都含有氧元素 |
BaCO3 BaCO3 . |
BaCO3为难溶性盐,其它盐易溶(或“BaCO3为钡盐,其它为钾盐.”) BaCO3为难溶性盐,其它盐易溶(或“BaCO3为钡盐,其它为钾盐.”) . |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 27.6 | 31.0 | 34.0 | 37.0 | x | 42.6 | 45.5 |
| 实验编号 | 实验1 | 实验2 | 实验3 | 实验4 |
| KCl质量/g | 5 | 15 | 25 | 35 |
| 溶液质量/g | 55 | 65 | 70 | 70 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?西城区一模)食盐在生产和生活中具有广泛的用途.
(2013?西城区一模)食盐在生产和生活中具有广泛的用途.| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
| 溶液质量/g | 209 | 236 | 272 | 272 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com