
下列说法正确的是( )。
A. 中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应
中和反应有盐和水生成,所以有盐和水生成的反应一定是中和反应
B.单质只含一种元素,所以含一种元素的物 质一定是单质
质一定是单质
C.离子是带电的原子或原子团,所以带电的微粒一定是离子
D.溶液是由溶质和溶剂组成,所以溶液一定是混合物
科目:初中化学 来源: 题型:
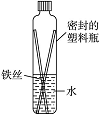
右图为某化 学兴趣小组同学设计的观察铁制品锈蚀的实验装置。请你分析以下相关叙述中,正确的是( )。
学兴趣小组同学设计的观察铁制品锈蚀的实验装置。请你分析以下相关叙述中,正确的是( )。
A.此实验设计必须在玻璃仪器中进行
B.一段时间后,塑料瓶会变瘪,说明铁生锈与空气有关
C.一段时间后,铁丝会由下到上出现锈蚀现象
D.一段时间后,水面处铁丝锈蚀严重,而水上、水下部分生锈不明显
查看答案和解析>>
科目:初中化学 来源: 题型:
请你从①甲醛、②亚硝酸钠、③黄曲霉素三种物质中,选择适当物质,将其序号填入相应空白处。
(1)容易被当作食盐而误食的有毒物质是____________。
(2)家庭装修材料中,容易挥发出的有毒物质是________。
(3)大米、花生、面粉等发生霉变而产生的有毒物质是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
以下两幅微观示意图揭示了化学变化的微观实质。相关说 法中正确的是( )。
法中正确的是( )。
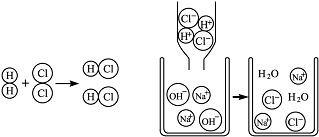
A.在化学变化中物质的质量是守恒的
B.原子在化学变化中是可以再分的
C.两幅图表示的都是化合反应
D.以上图示中未涉及中和反应
查看答案和解析>>
科目:初中化学 来源: 题型:
关于下列四种粒子的结构示意图的说法中正确的是
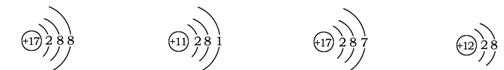
① ② ③ ④
A.①③属于不同种元素 B.②表示的元素在化合物中通常显+1价
C.②③的化学性质相似 D.④属于离子,离子符号为Mg+2
查看答案和解析>>
科目:初中化学 来源: 题型:
对比学习有利于发现事物的共性与个性。为探究酸的化学性质,同学们进行了如下实验:
| 实验内容 | 实验现象 | 分析与结论 |
|
| 装有醋酸晶体 | 酸的很多反应通常在水溶液中才能完成。 |
| 用玻璃棒蘸硫酸在白纸上写字 | (填“浓”或“稀”)硫酸使白纸炭化。 | 即使是同种酸,由于 不同,它们的性质不完全相同。 |
|
| 两试管中均产生 | 不同的酸具有相似的性质,这是因为酸的溶液中都含有 (填化学符号)。 |
|
| E试管中产生 , | 不同的酸根会导致酸的“个性”差异。因此,可用氯化钡溶液鉴别盐酸和硫酸。 |
清洗试管时,小乔同学将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。请分析上述现象并回答:
Ⅰ.废液缸中产生气体的化学方程式为 。
Ⅱ. 废液缸里最终产生的白色沉淀一定有 (填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂。该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体。
 一、【提出问题】该白色固体是什么?
一、【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠 猜想b:碳酸氢钠
小周同学认为猜想b不成立,理由是反应物中没有  元素。
元素。
【实验】取少量生成的白色固体于试管中,加入 ,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊。
稀盐酸(稀HCl)
【结论】猜想a成立。
请写出过氧化钠与二氧化碳反应的化学方程式 。
小周在查阅资料的过程中发现过氧化钠固体还能与水反应放出氧气。实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,该兴趣小组决定取3.00g变质粉末继续探究其中的成分及其质量。
二、【提出问题】变质的过氧化钠粉末中有哪些成分,它们的质量是多少?
【查阅资料】
① 2Na2O2+2H2O═4NaOH+O2↑ ②碳酸钠溶液显碱性,氯化钙溶液显中性。
③ Na2CO3+ CaCl2═CaCO3↓+2 NaCl
【猜想与假设】
(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是 的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
……
【设计实施方案】
| 实验步骤 | 实验现象 |
| ①取3.00g变质粉末于一支大试管内,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体。 | 固体完全溶解,______________________ |
| ②继续向上述试管中加入足量的石灰水,充分反应。 | __________________________________ |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g。 |
【解释与结论】同学们经过认真分析,得出了以下结论。
粉末中含有的成分及质量:
| Na2O2 | NaOH | Na2CO3 | |
| 成分(填“有”或“没有”) | |||
| 质量(g) |
【反思与评价】
(1)实验室在保存过氧化钠时应注意_______________。
(2)有同学提出把第②步实验中足量的石灰水改为足量氯化钙溶液,至沉淀不再生成时过滤,向滤液中滴加无色酚酞试液,若液体变红,则证明原粉末中有NaOH。你认为该方案是否合理并说明理由____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com