
| A. | 少量面粉放入足量水中并充分搅拌,能形成均一、稳定的溶液 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体 | |
| C. | 铁丝在空气中燃烧,火星四射,放出热量,生成一种黑色固体 | |
| D. | 在燃着的蜡烛火焰上方放置一玻璃片,有黑色固体生成 |
分析 A、根据面粉难溶于水,进行分析判断.
B、根据硫在空气中燃烧的现象进行分析判断.
C、根据铁丝在空气中燃烧的现象进行分析判断.
D、根据蜡烛燃烧进行分析判断.
解答 解:A、面粉难溶于水,少量面粉放入足量水中并充分搅拌,不能和水形成均一、稳定的混合物,即不能够形成溶液,故选项说法错误.
B、硫在空气中燃烧,产生淡蓝色火焰,产生一种具有刺激性气味的气体,故选项说法错误.
C、铁丝在空气中只能烧至发红,不会产生火星,故选项说法错误.
D、蜡烛不充分燃烧会有炭黑生成,在燃着的蜡烛火焰上方放置一玻璃片,有黑色固体生成,故选项说法正确.
故选:D.
点评 本题难度不大,掌握常见物质燃烧的现象、溶液的本质特征(均一性、稳定性、混合物)即可正确解答,在描述物质燃烧的现象时,需要注意光和火焰、烟和雾的区别.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:选择题
| A. | Mg | B. | MgO | C. | Mg(OH)2 | D. | MgCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
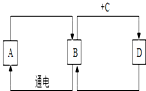 已知A、B、C、D是初中化学常见的物质.它们之间的相互转化关系如图所示,其中A是相同条件下密度最小的气体,B在常温下是一种无色液体,C可用于灭火.(部分反应物、生成物和反应条件未标出)请回答下列问题:
已知A、B、C、D是初中化学常见的物质.它们之间的相互转化关系如图所示,其中A是相同条件下密度最小的气体,B在常温下是一种无色液体,C可用于灭火.(部分反应物、生成物和反应条件未标出)请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).
已知A、B、C、D、E是初中化学常见的不同类别的物质,C的水溶液呈蓝色,D是一种红色固体,B→D的反应过程较为复杂,D→B的反应用于冶金工业,图中“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com