
分析 理解酸的定义:酸是在水溶液中电离出的阳离子全部是氢离子的化合物,据浓硫酸具有吸水性和脱水性,浓盐酸具有挥发性,进行分析解答.
解答 解:因为酸是在水溶液中电离出的阳离子全部是氢离子的化合物,所以酸在水溶液中具有相同的H+;
实验室中浓H2SO4需要密封保存,原因是浓H2SO4具有吸水性.
用玻璃棒蘸取少量浓硫酸在滤纸上写字,过后观察,字迹显黑色,这主要是由于浓硫酸具有脱水性,将滤纸中的氢、氧元素以水的形式夺走,导致纸张炭化.
若打开浓盐酸的瓶盖,发现瓶口冒白雾,是因为浓盐酸具有挥发性,从浓盐酸中挥发出来的氯化氢气体与空气中的水蒸气结合成盐酸小液滴,因此浓盐酸也要密封保存.
故答案为:H+;吸水;脱水;挥发.
点评 本题难度不大,掌握浓硫酸具有吸水性与脱水性、浓盐酸具有挥发性是正确解答本题的关键.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:解答题
| 元素名称 | 氢 | 氧 | 氯 | 锰 | 铁 |
| 元素符号 | H | O | Cl | Mn | Fe |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 方案 | 步骤 | 现象 | 结论 |
| Ⅰ | ①取样品,滴加BaCl2溶液 ②对步骤①反应后的混合物进行过滤,在滤渣中滴加稀盐酸 | ①有白色沉淀产生 ②无明显现象 | 废液中含有SO42- |
| Ⅱ | ①取样品,滴加过量盐酸 ②在步骤①的溶液中滴加BaCl2溶液 | ①无明显现象 ②有白色沉淀产生 | 废液中含有SO42- |
| Ⅲ | ①取样品,滴加Ba(NO3)2溶液 ②对步骤①产生的混合物进行过滤,在滤渣中滴加稀硝酸 | ①有白色沉淀产生 ②无明显现象 | 废液中含有SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 关于水的电解实验,下列说法正确的是( )
关于水的电解实验,下列说法正确的是( )| A. | 这个实验证明了水是由氧气和氢气组成的 | |
| B. | 电解水生成的氢气和氧气质量比为2:1 | |
| C. | 水电解是化学变化 | |
| D. | 实验证明水是一种混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
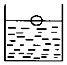 如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )
如图在室温下的饱和硝酸钾溶液中放了一个塑料小球.以下做法能使小球下沉的是( )| A. | 加入少量硝酸钾晶体,充分搅拌 | B. | 蒸发一些溶剂,恢复到室温 | ||
| C. | 升高温度,使硝酸钾晶体析出 | D. | 降低温度,使硝酸钾晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
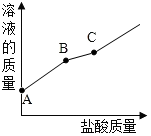 科学就在我们身边,科学知识与我们的生活息息相关.
科学就在我们身边,科学知识与我们的生活息息相关.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com