
分析 石蕊试液遇酸性溶液变红色,遇中性溶液不变色,遇碱性溶液变蓝.
解答 解:①因为酸能使紫色石蕊变红,中性物质不能使紫色石蕊变色,蒸馏水是由水分子构成的.所以在第一支洁净的试管里加入约2mL蒸馏水,滴人几滴紫色石蕊试液,观察到的现象是颜色无变化,说明H2O分子不能使石蕊变色;
②氯化钠溶液呈中性,含有Na+Cl-滴入几滴紫色石蕊试液不变色,说明这两种微粒都不能使紫色石蕊试液变色;
③盐酸能使紫色石蕊变红色,由前两个实验知H2O分子和Cl-都不能使紫色石蕊试液变红色,而在盐酸中只含有H+Cl-和H2O分子三种微粒,所以只有H+能使紫色石蕊试液变红色;
故答案为:
①溶液无变化;H2O不能使石蕊变色;
②不能使石蕊变色;
③紫色石蕊试液变红; H+使石蕊变色
点评 本题以实验探究的方式来考查酸溶液使石蕊变红的原因,学生应注重实验中现象的观察,将现象和粒子结合来分析解决问题,从而得出正确的结论,学生应注重探究的学习过程.


科目:初中化学 来源: 题型:解答题
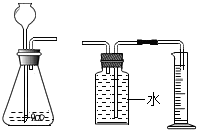 为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:
为了探究金属与酸反应的速率与哪些因素有关,小谷进行了以下实验探究:| 实验步骤 | 现象 | 结论 |
| ①将足量铁粉与锌粉分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率: Fe>Zn | 反应速率与反应物的金属的活动性强弱有关 |
| ②将等质量锌粉与锌片分别放入10%100mL稀硫酸中,观察现象 | 产生气泡速率: 锌粉>锌片 | 反应速率与反应物的接触面积大小有关 |
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积 | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 表示离子个数的是⑤⑥ | B. | 表示离子所带电荷数的是④⑤ | ||
| C. | 表示分子中原子个数的是③⑦ | D. | 表示分子个数的是①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com