
分析 【猜想】
氢氧化钙和稀盐酸反应生成氯化钙和水;
【进行实验】
氢氧化钙溶液显碱性,能使酚酞试液变红色;
氯化钙显中性,不能使酚酞试液变色,稀盐酸显酸性,不能使酚酞试液变色;
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,能够氯化钙反应生成白色沉淀碳酸钙和氯化钠;
【反思与拓展】
发生化学反应时,反应物不一定恰好完全反应;
利用pH试纸可以测定溶液的酸碱度;
铜不能和稀盐酸反应;
显酸性的溶液能使石蕊试液变红色;
氯离子能和银离子结合成白色沉淀氯化银;
稀盐酸能和水泥砂石反应,也能和铁制管道反应.
解答 解:【猜想】猜想一:可能是CaCl2和Ca(OH)2;猜想二:可能只有CaCl2;猜想三:可能是CaCl2和HCl.
故填:可能是CaCl2和HCl.
【进行实验】
实验步骤:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡;
实验现象:酚酞试液不变色;结论:猜想一不正确;
实验步骤:实验步骤取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量;
实验现象:先产生气泡,后产生白色沉淀; 结论:猜想二不正确,猜想三正确.
故填:酚酞试液不变色;先产生气泡,后产生白色沉淀.
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量.
故填:反应物是否过量.
(2)a.利用pH试纸测定溶液的酸碱度,如果pH小于7,说明含有稀盐酸,如果pH等于或大于7,则溶液中不含有稀盐酸,因此能够完成实验;
b.铜不能和稀盐酸反应,因此不能完成实验;
c.滴加紫色石蕊溶液时,如果石蕊试液变红色,说明溶液中含有稀盐酸,如果溶液变蓝色,或不变色,说明溶液中不含有稀盐酸,因此能够完成实验;d.硝酸银溶液能和氯化钙反应生成硝酸钙和氯化银沉淀,能和稀盐酸反应生成硝酸和氯化银沉淀,因此不能完成实验.
故填:ac.
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是腐蚀下水道;
要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的碳酸钙,这是因为碳酸钙不溶于水,当稀盐酸完全反应后,碳酸钙不再溶解.
故填:腐蚀下水道;碳酸钙.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | 1:2 | B. | 1:4 | C. | 3:20 | D. | 3:40 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
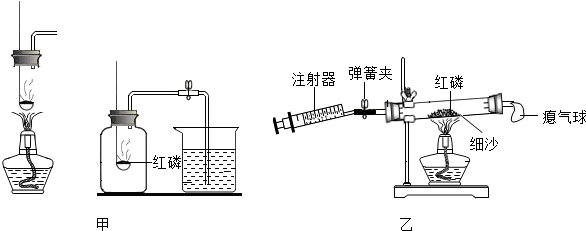
| 玻璃管中原有 空气的体积 | 注射器中气体的体积 | 结论 | |
| 反应前 | 反应后 | ||
50mL | 40 mL | 30 mL | 氧气约占空气体积的五分之 |
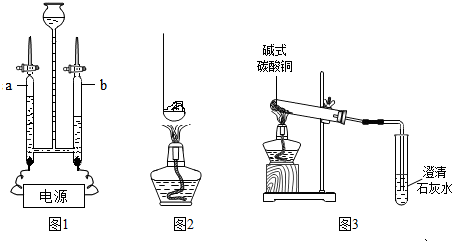
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | 安全常识 | B | 数据记录 |
| 天然气泄漏立即打开换气扇 炒菜时油锅着火--用锅盖盖灭 预防煤气中毒--确保烟道畅通 | 量筒量液体-体积为9.1mL 托盘天平称固体-质量为5.2g pH试纸测酸雨-pH为4.5 | ||
| C | 物质的性质与用途 | D | 化学反应的条件 |
| N2化学性质稳定--作保护气 H2具有可燃性--作气体燃料 CO具有还原性--冶炼金属 | 实验室制氧气--一定需要催化剂 燃烧--接触氧气、温度达着火点 复分解反应-生成气体、沉淀或水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com