
 现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生产沉淀的质量与加入NaOH溶液的质量关系如图所示.
现有含HCl和CuCl2的混合溶液50g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生产沉淀的质量与加入NaOH溶液的质量关系如图所示.分析 (1)根据氢氧化钠与盐酸反应生成氯化钠和水,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,还需要结合a点时氢氧化钠过量进行分析;
(2)氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,根据沉淀的质量计算出氯化铜的质量,再用氯化铜的质量除以50g即可;
(3)根据沉淀质量计算出与氯化铜反应的氢氧化钠的质量,再除以氢氧化钠的质量分数,算出与氯化铜反应的氢氧化钠溶液的质量再加上与盐酸反应的氢氧化钠溶液质量40g即可.
解答 解:(1)氢氧化钠与盐酸反应生成氯化钠和水,氢氧化钠与氯化铜反应生成氢氧化铜沉淀和氯化钠,所以反应后溶液中的溶质一定含有氯化钠,a点时氢氧化钠过量,所以溶质中还含有氢氧化钠;
(2)设生成9.8g沉淀需要参加反应的氯化铜的质量为x,参加反应的氢氧化钠的质量为y则:
CuCl2+2NaOH═Cu(OH)2↓+2NaCl,
135 80 98
x y 9.8g
$\frac{135}{x}=\frac{80}{y}=\frac{98}{9.8g}$
解得x=13.5g,y=8g,
混合溶液中CuCl2的质量分数:$\frac{13.5g}{50g}$×100%=27%;
(3)与氯化铜反应的氢氧化钠溶液质量为:$\frac{8g}{10%}$=80g,所以恰好完全反应时,消耗NaOH溶液的总质量:40g+80g=120g.
故答案为:(1)NaCl、NaOH;(2)27%;(3)120g.
点评 本题考查化学方程式与溶液的综合计算,解题关键是分析清楚反应过程的先后,找出每个过程中已知物质的质量.要知道加入的氢氧化钠先与盐酸反应,把盐酸反应完了再与氯化铜反应.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | pH<5.6的雨水称为酸雨 | |
| B. | PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性 | |
| C. | “温室效应”主要是由CO2等气体引起的 | |
| D. | 加速石油、煤炭的开采,快速提高人类的生活质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤出的固体中一定含有银,可能含有铜、锌 | |
| B. | 滤出的固体中一定含有银和铜,可能含有锌 | |
| C. | 滤液中一定含有硝酸铝、硝酸锌,一定没有硝酸铜和硝酸银 | |
| D. | 加入铝粉反应后得到滤液的质量大于反应前滤液的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 油脂.糖类、蛋白质都是人体必需的营养素,撬入得越多越好 | |
| B. | 为防止水污染,应禁止使用化肥和农药 | |
| C. | 吃水果和蔬菜可以补充维生素 | |
| D. | 用洗洁精去油污是因为洗洁精能溶解油污 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
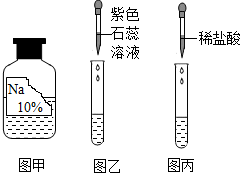 同学们在化学学习中发现,不同物质的变化常伴随相同的实验现象,但从化学的角度去研究,会发现其有本质的区别.
同学们在化学学习中发现,不同物质的变化常伴随相同的实验现象,但从化学的角度去研究,会发现其有本质的区别.| 操作步骤 | 相同的现象 | 分析与解释 | |
| 实验一 | 如图所示,向小试管中加入适量氢氧化钠固体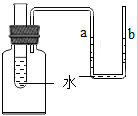 | U形管中液面a下降,b升高 | 两个实验中,其中一个实验发生了化学变化,其化学方程式是 CaO+H2O=Ca(OH)2;另一个实验没有发生化学变化 |
| 实验二 | 用氧化钙代替氢氧化钠固体重复一次上述实验 |
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下稀溶液的pH | 7 | 13 | 11 | 9 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH溶液(Na2SO4) | 加入适量的Ba(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 高温加热至固体质量不变 |
| C | CO2(CO) | 通入氧气流并点燃 |
| D | CuSO4溶液(H2SO4) | 加足量氧化铜粉末,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
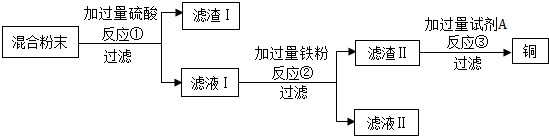
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com