
 =
= =
=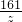 =
=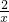
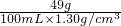 ×100%=37.7%
×100%=37.7% ×100%=49.8%
×100%=49.8%

 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:
| 硫酸 化学纯(CP) (500mL) 品名 硫酸 化学式 H2SO4 相对分子质量 98 密度 1.84g/cm3 质量分数 98%(1)该试剂瓶中硫酸溶液的质量是 (2)欲配制100g溶质质量分数为19、6%的稀硫酸,需这种浓硫酸多少克? (3)取足量的稀硫酸与6.5g锌充分反应,可制得氢气多少克? 查看答案和解析>> 科目:初中化学 来源: 题型:解答题 实验室中浓硫酸的商标如图所示.请根据有关信息计算:
(2)欲配制100g溶质质量分数为19、6%的稀硫酸,需这种浓硫酸多少克? (3)取足量的稀硫酸与6.5g锌充分反应,可制得氢气多少克? 查看答案和解析>> 科目:初中化学 来源:山西 题型:问答题 实验室中浓硫酸的商标如图所示.请根据有关信息计算:
(2)欲配制100g溶质质量分数为19、6%的稀硫酸,需这种浓硫酸多少克? (3)取足量的稀硫酸与6、5g锌充分反应,可制得氢气多少克? 查看答案和解析>> 科目:初中化学 来源:2009-2010学年年山西省太原市师院附中九年级(下)月考化学试卷(解析版) 题型:解答题 实验室中浓硫酸的商标如图所示.请根据有关信息计算:
(2)欲配制100g溶质质量分数为19、6%的稀硫酸,需这种浓硫酸多少克? (3)取足量的稀硫酸与6.5g锌充分反应,可制得氢气多少克? 查看答案和解析>> 科目:初中化学 来源:2006-2007学年甘肃省兰州市九年级(上)期末化学试卷(解析版) 题型:解答题 实验室中浓硫酸的商标如图所示.请根据有关信息计算:
(2)欲配制100g溶质质量分数为19、6%的稀硫酸,需这种浓硫酸多少克? (3)取足量的稀硫酸与6.5g锌充分反应,可制得氢气多少克? 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |