
工业上用“侯氏制碱法”制得的纯碱中常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的质量分数,三位同学分别设计了甲、乙、丙三套实验装置(如图所示).测定的方法是:取一定质量的纯碱样品,加入足量的稀硫酸,产生的二氧化碳气体用足量的氢氧化钠溶液吸收,根据氢氧化钠溶液(盛装在甲、乙、丙中的Ⅰ、Ⅱ、Ⅲ瓶中)在实验前后的质量差,通过计算,确定碳酸钠的质量分数.操作时,甲、丙装置中气囊内的空气可以根据需要排出装置中的气体.在滴加稀硫酸前,连接甲、乙、丙装置的a、b管口.
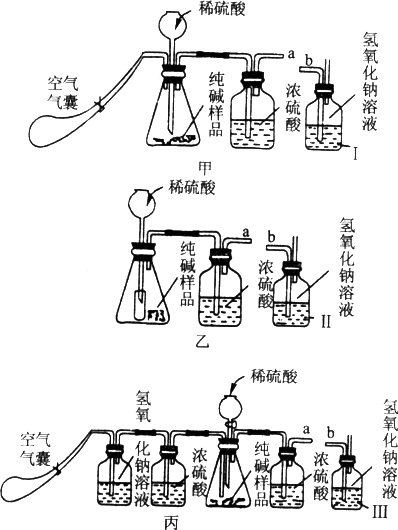
上述装置中,________(填“甲”、“乙”或“丙”)装置能比较准确测得样品中碳酸钠的质量分数.请分别指出另外两套装置的一点不足:________.
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
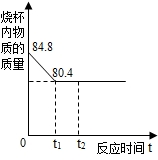 工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题:
工业上用侯氏制碱法制得的纯碱样品中含有一定量的氯化钠.现称取只含有氯化钠杂质的纯碱样品11.8g放入盛73g稀盐酸的烧杯中,恰好完全反应.反应过程中烧杯内物质的质量随时间的变化关系如图所示.试回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 温度 盐 溶解度 |
10℃ | 20℃ | 30℃ | 40℃ | 50℃ |
| NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NH4HCO3 | 15.8 | 21.0 | 27.0 | ------ | ------ |
| NaHCO3 | 8.1 | 9.6 | 11.1 | 12.7 | ---- |
| NH4Cl | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com