
 活动与探究课上,某实验小组的同学对失去标签的①稀盐酸②氢氧化钠③碳酸钠④氢氧化钙四瓶溶液进行鉴别时,他们按照讨论的方案,分别取四种溶液各少量进行两两混合的实验.
活动与探究课上,某实验小组的同学对失去标签的①稀盐酸②氢氧化钠③碳酸钠④氢氧化钙四瓶溶液进行鉴别时,他们按照讨论的方案,分别取四种溶液各少量进行两两混合的实验.| 两两混合 | A+B | B+C | C+D | A+D |
| 实验现象 | ↑ | ↓ | / | / |


科目:初中化学 来源: 题型:
| 实验装置 | 实验现象 | 实验结论 |
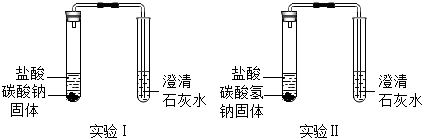 | 实验Ⅰ、Ⅱ中均观察到:白色固体逐渐减少, | Na2CO3和NaHCO3都能与盐酸反应产生CO2;NaHCO3与盐酸反应的化学方程式是 |
| t1/℃ | t2/℃ | t3/℃ | |
| Na2CO3 | 23.3 | 20.0 | 23.7 |
| NaHCO3 | 18.5 | 20.0 | 20.8 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
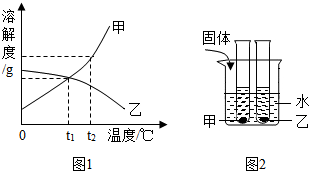 图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发).根据图象和有关信息填空:
图1是甲、乙两种固体物质的溶解曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发).根据图象和有关信息填空:查看答案和解析>>
科目:初中化学 来源: 题型:
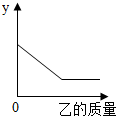 甲为初中化学常见物质,请根据下列叙述回答问题.
甲为初中化学常见物质,请根据下列叙述回答问题.| 甲 | 乙 | y轴含义 | |
| A | 生石灰 | 水 | 固体质量 |
| B | 铜锌合金粉末 | 硫酸铜溶液 | 溶液质量 |
| C | 工业炼铁的尾气 | 氢氧化钠溶液 | 气体质量 |
| D | 密闭容器中的空气 | 红磷 | 反应过程中容器内压强 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 选项 | 实验目的 | 实验操作 |
| A | 除去Cu中的Fe | 过量AgNO3溶液 |
| B | 除去NaOH中的Ca(OH)2溶液 | 加过量Na2CO3溶液 |
| C | 除去CaO中的CaCO3 | 高温灼烧 |
| D | 除去CO2中的CO | 通入过量NaOH溶液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com