
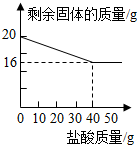
 某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称量,各次稀盐酸用量和剩余固体质量记录如下:
某化学兴趣小组的同学为测定假黄金(铜锌合金)组成元素的质量分数,称取20克假黄金置于烧杯中,用某浓度的稀盐酸50克,分5次加入,每次充分反应后,取出固体,经过滤、干燥等操作后称量,各次稀盐酸用量和剩余固体质量记录如下:| 实验次数 | 加入稀盐酸的用量/g | 剩余固体的质量/g |
| 1 | 10 | 19 |
| 2 | 10 | 18 |
| 3 | 10 | 17 |
| 4 | 10 | 16 |
| 5 | 10 | 16 |
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 干冰放置在蒸发皿上,固体逐渐减少最后消失----升华 | |
| B. | 打开装有浓盐酸的试剂瓶瓶盖,瓶口出现白雾----挥发 | |
| C. | 用洗涤剂洗去餐具上的油污----溶解 | |
| D. | 利用沸点的差异,从石油中分离各组分----分馏 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
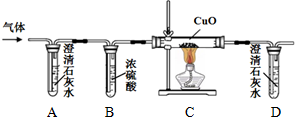
 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com