
| A. | 菱铁矿是铁的合金 | |
| B. | 菱铁矿中铁元素的质量分数为48.3% | |
| C. | FeCO3中铁的化合价为+3 | |
| D. | FeCO3是含有氧元素的化合物 |
分析 A、根据菱铁矿的主要成分是FeCO3,进行分析判断.
B、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,菱铁矿的主要成分是FeCO3,进行分析判断;
C、根据在化合物中正负化合价代数和为零,进行分析判断.
D、根据由不同种元素组成的纯净物是化合物,进行分析判断.
解答 解:A、菱铁矿的主要成分是FeCO3,不是铁的合金,故选项说法错误.
B、FeCO3中铁元素的质量分数为$\frac{56}{56+12+16×3}$×100%≈48.3%,但菱铁矿的主要成分是FeCO3,含有杂质,则菱铁矿中铁元素的质量分数不等于48.3%,故选项说法错误.
C、碳酸根显-2价,设FeCO3中铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)=0,则x=+2价,故选项说法错误.
D、FeCO3是由铁、碳、氧三种元素组成的纯净物,属于化合物,故选项说法正确.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算等进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 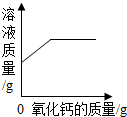 常温下,向一定量的饱和石灰水中加入氧化钙 常温下,向一定量的饱和石灰水中加入氧化钙 | |
| B. | 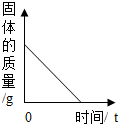 一氧化碳还原一定质量的氧化铜 一氧化碳还原一定质量的氧化铜 | |
| C. | 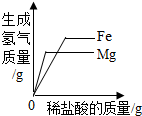 向等质量的铁和镁中分别加入足量的稀盐酸 向等质量的铁和镁中分别加入足量的稀盐酸 | |
| D. | 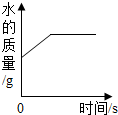 向一定质量的过氧化氢的水溶液中加入二氧化锰 向一定质量的过氧化氢的水溶液中加入二氧化锰 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com