
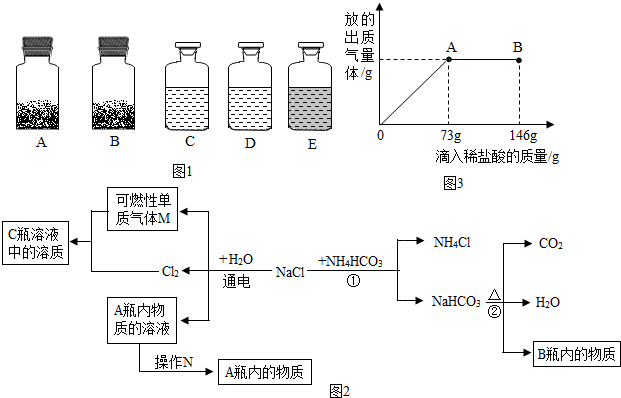
分析 (1)根据酸的性质可知,浓硝酸见光易分解,则应保存在棕色试剂瓶,利用浓盐酸易挥发,而浓硫酸不挥发来区分;
(2)根据框图中的反应和利用元素守恒的方法来确定物质及相关的问题;
I、碳酸氢钠受热后生成了水、二氧化碳和B,根据质量守恒定律可知,B是碳酸钠,并写出反应的方程式;
II、根据反应①中的反应物和生成物的特点进行分析,根据操作N可以将固体从液体分离来分析,
III、根据氢氧化钠溶于水有明显的温度变化进行分析,
(3)根据图象不难看出,当滴加稀盐酸至图中A点时,生成的气体的质量不再增加,说明碳酸钠已刚好完全反应,若再加稀盐酸则表明盐酸已过量,即说明参加反应的稀盐酸的量是73g,把稀盐酸中溶质的质量代入化学方程式进行计算就可求出有关的量;求反应后所得的质量可以根据加入物质的总质量-难溶于水也不参加反应的杂质的质量-生成的气体或沉淀的质量.
解答 解:(1)因浓硝酸易见光分解,浓盐酸易挥发.故答案为:浓硝酸;看到C瓶的瓶口冒白雾,D瓶的瓶口无现象(写冒白烟错误);说明C瓶内的是浓盐酸,D瓶内的是浓硫酸;故答案为:浓硝酸;C瓶的瓶口冒白雾,D瓶的瓶口无现象;
(2)Ⅰ.根据质量守恒定律可知,碳酸氢钠在受热后分解成碳酸钠、水和二氧化碳,故答案为:Na2CO3;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
Ⅱ.①反应是两种化合物反应生成了两种化合物的反应,满足复分解反应的条件,蒸发是使固体从液体之后析出的一种操作方法,A瓶内物质的溶液经过操作N分离出了固体,故答案为:复分解反应;蒸发结晶;
Ⅲ.氢氧化钠在水中溶解时会放出大量的热,无明显变化的是碳酸钠,故答案为:分别从两瓶内取少量固体溶于水,明显放热的为NaOH,否则为Na2CO3;因为碳酸钠溶液也显碱性,能使酚酞试液变成红色,因此不能用酚酞试液区分;
(3)①从图象中不难看出,当滴加稀盐酸到A时,二氧化碳的质量不再增加,说明碳酸钠已完全反应,若再滴加稀盐酸,则盐酸过量,溶液呈酸性,PH小于7.故填:<
②73g10%的稀盐酸中含HCl的质量是:73g×10%=7.3g,设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y,生成的二氧化碳的质量为z.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 73 117 44
x 7.3g y z
$\frac{106}{x}$=$\frac{73}{7.3g}$,x=10.6g
$\frac{73}{7.3g}$=$\frac{117}{y}$,y=11.7g
$\frac{73}{7.3g}$=$\frac{44}{x}$,z=4.4g
原混合物中碳酸钠的质量为10.6g.
烧杯里不饱和溶液中溶质的质量为:11.7g+(20.4g-10.6g)=21.5g
烧杯里不饱和溶液的质量为:20.4g+73g-4.4g=89g
烧杯里不饱和溶液中溶质的质量分数为:$\frac{21.5g}{89g}$×100%=24.2%
答:溶质的质量分数为24.2%.
故答案为:①<;②24.2%.
点评 本题考查知识点多,利用的方法是常用的方法,通过本题应掌握物质的区分和转化,并根据化学方程式进行计算和有关溶液中溶质质量分数的计算,从而培养学生对概念的应用和分析问题、解决问题的能力.


 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | Z<Y<X | B. | X<Z<Y | C. | Y<X<Z | D. | X<Y<Z |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ①②⑤④③ | D. | ⑤②④①③ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | KNO3、NaOH、HCl | B. | Ca(OH)2、HCl、NaCl | ||
| C. | HNO3、KOH、CuSO4 | D. | H2SO4、Na2CO3、Ba(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com