
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取样于试管中,滴加稀盐酸,充分振荡 | 有 生成 | 原溶液中一定含有碳酸钙 |
| (2)另取样于试管中,滴加酚酞试液 | 溶液呈红色 | 原溶液中含有 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作 | 实验现象 | 实验结论 |
| A.将样品研碎放入水中,充分搅拌,静置。 | 底部有大量白色不溶物出现 | 白色固体中含有碳酸钙 |
| B.取上层清液,滴加无色酚酞试液。 | 溶液变为 | 白色固体中含有氢氧化钙 |
| 实验操作 | 实验现象 | 实验结论 |
| 1.取样品放入盛有水的试管中,用温度计测量水温先后的情况 | 温度升高 | |
| 2.取样品放入研钵,与硝酸铵一起碾磨 | | 白色固体中含有氢氧化钙 |
| 3.取样滴加稀盐酸 | 有气泡产生 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的_________。 | 实验过程中始终没有气泡产生。 | 则证明猜想 成立。 |
| 步骤二:另取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氯化钡溶液。 | 实验过程中产生 | 则证明猜想Ⅱ或Ⅲ成立。此过程中发生反应的化学方程式为 _____________________ |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
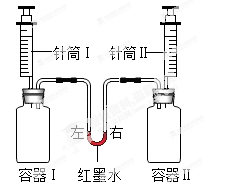
| 实验编号 | 容器I | 针筒I | 容器II | 针筒II | 红墨水液面位置 |
| a | 二氧化碳(充满) | 10mL澄清石灰水 | 二氧化碳(充满) | 10mL水 | 保持左高右低 |
| b | 0.55g锌 | 15mL盐酸 | 0.24g镁 | 15mL盐酸 | |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.氧化铜和木炭:看颜色 | B.铝与铝合金:比较硬度 |
| C.硬水与软水:加明矾 | D.:滴入紫色石蕊溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 实验操作 | 实验现象 |
| (1)取少量样品于试管中,慢慢滴加BaCl2溶液 | 出现白色沉淀 |
| (2)静置一段时间后,倾去上层清液,向沉淀中继续滴加稀盐酸 | 白色沉淀全部溶解,产生大量气泡 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com