
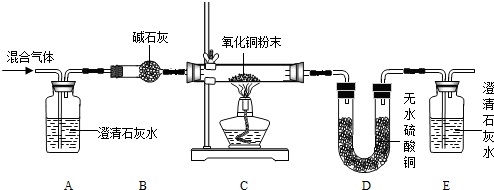
ij�о�С���ͬѧ������ͼװ�ý���ʵ�飬����۲쵽����������ˮ�еİ����ۻ���һ��ɫҺ�Σ����ã�ͭƬ�ϵİ���ʼȼ�գ�������ˮ�еİ�����ȼ�ա���ش�
(1)��ͭƬ�ϵĺ���û��ȼ�գ�����Ϊ ��
(2)ʵ����ϣ����ձ��е���ˮ����������ˮ�쵹��ʱ�����ְ���¶��ˮ��;��ҡ�ȼ������������ʹ����� ��
(3)��ȼ��ȼ����Ҫͬʱ����������� ��
(4)ͨ�������������ķ����� ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
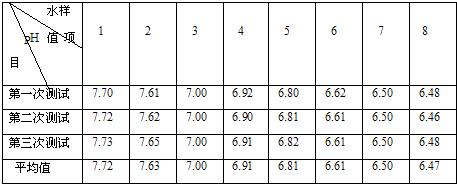
| ˮ�� PHֵ ��Ŀ |
1 | 2 | 3 | 4 |
5 |
6 | 7 | 8 |
| ��һ�β��� | 7.70 | 7.61 | 7.00 | 6.92 | 6.80 | 6.62 | 6.50 | 6.48 |
| �ڶ��β��� | 7.72 | 7.62 | 7.00 | 6.90 | 6.81 | 6.61 | 6.50 | 6.46 |
| ������� | 7.73 | 7.65 | 7.00 | 6.91 | 6.82 | 6.61 | 6.50 | 6.48 |
| ƽ��ֵ | 7.72 | 7.63 | 7.00 | 6.91 | 6.81 | 6.61 | 6.50 | 6.47 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com