
【题目】甲、乙、丙三种物质的溶解度曲线如图所示。下列说法错误的是( )
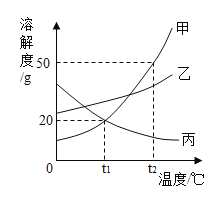
A. t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是:乙>甲=丙
B. t2℃时,30g甲物质加入50g水中,充分搅拌后,所得溶液的溶质的质量分数为37.5%
C. 将相同质量的甲、乙、丙三种物质的饱和溶液从t2℃降温到t1℃,析出晶体最多的是甲
D. 欲将丙物质的不饱和溶液变为饱和溶液,可以采取升高温度的方法
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:初中化学 来源: 题型:
【题目】下列有关溶液的说法中,正确的是( )
A. 饱和溶液一定比不饱和溶液所含的溶质多
B. 升高温度或增大压强均可以增大气体在水中的溶解度
C. 将100g溶质质量分数为![]() 的氯化钠溶液稀释至
的氯化钠溶液稀释至![]() ,需要加水100g
,需要加水100g
D. 将一定质量某物质的饱和溶液降温析出晶体后,所得溶液中溶质的质量一定减小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图A是某粒子的结构示意图,B是铝元素周期表中的信息。请回答下列问题:
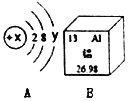
(1)若A粒子带有两个单位的负电荷,且y等于8,则该粒子的符号为______;
(2)当x=17时,A元素和B元素形成的化合物化学式______;
(3)B元素的单质在空气中能生成致密的______(化学式)薄膜;
(4)从B中可知,铝的相对原子质量为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】a,b两种物质的溶解度曲线如图所示,下列说法正确的是 ( )

A. a物质的溶解度大于b物质的溶解度
B. t1℃时,a,b两溶液的溶质质量分数相等
C. 将t2℃时a的饱和溶液降温至t1℃,溶液质量不变
D. 将t1℃时,a、b物质的饱和溶液升温至t2℃时,两溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验回答问题。
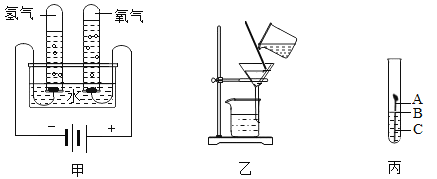
(1)如图甲所示是电解水的实验,根据实验中只生成氢气和氧气,确定水是由_____组成的。得出结论的依据是_____,写出水电解的化学方程式_____。
(2)如图乙所示是粗盐提纯实验中的过滤操作。过滤时,最好先将上层液体倒入过滤器,然后再倒入混有沉淀的液体,以免_____,使过滤速度过慢。在粗盐提纯实验中,若颠倒液体时液面高于滤纸边缘 (其他操作均正确)。则得到的精盐质量会_____ (选填“偏大”“不变”或“偏小”)。操作过程中,玻璃棒的作用是_____。
(3)如图,取一根约10cm的光亮铁钉放在自来水中,观察A、B、C三处的变化。几天后,他们会发现_____处最先出现铁锈,大家结合书本知识知道,铁在空气中生锈实际是铁和_____、_____等物质相互作用发生一系列复杂的化学反应的过程。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国是把香椿当做蔬菜的唯一国家,它不仅营养丰富,而且具有极高的药用价值,如香椿中含有的皂甙,具有抗菌、防癌的作用,皂甙的化学式为C27H42O3,请你计算:
(1)皂甙属于_______________(填“有机物”或“无机物”);
(2)皂甙中各元素的质量之比是____________________(最简整数比);
(3)含氢元素8.4 g的皂甙的质盆为________________克(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】推理是一种重要的学习方法。下列推理得出的相关结论正确的是( )
A. 含碳元素的物质充分燃烧会生成![]() ,所以燃烧能生成
,所以燃烧能生成![]() 的物质一定含碳元素
的物质一定含碳元素
B. 铁丝在氧气中能够燃烧,空气中有氧气,所以铁丝在空气中一定能够燃烧
C. 二氧化碳能使燃着木条熄灭,所以能使燃着木条熄灭的气体一定是二氧化碳
D. 水与过氧化氢都是由氢、氧元素组成的化合物,所以它们的性质完全相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是由氢、氧两种元素组成的化合物,这一结论是科学家们在大量实险的基础上得出的。
(资料)(1)碱石灰的主要成分是氢氧化钠(NaOH)和氧化钙(CaO),可吸水,并与二氧化碳反应;
(2)同温同压下,气体的体积比等于分子数比。
(1)研究氢气的燃烧实验是人们认识水组成的开始。
①氢气在点燃前一定要_____。
②在相同条件下,欲使1L氢气完全燃烧,所需空气至少约为_____L。
(2)科学家们又用“电解法”证明了水的组成(如图),该反应的化学方程式为_____________。电解时,水中需加入少量稀硫酸或氢氧化钠溶液,其作用是___________。通电一段时间后, 量筒乙中收集到的气体是____________(填物质名称),若发现甲、乙两量筒中收集的气体体积比略小于 1:2,其原因可能是___________________(写出一条即可)。
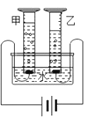
(3)拉瓦锡还用另一实验证明了水的组成。他让水蒸气通过一根烧红的铁质枪管,结果得到了氢气,同时枪管表面有黑色固体(磁铁矿的主要成分)生成。该反应的化学方程式为_____________。
(4)用“氢气还原氧化铜”实验也可以证明水的组成(如图)。
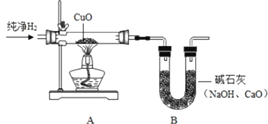
①如图连接实验装置、检查装置的气密性、装药品、固定实验装置后,主要实验步骤有: a.通入氢气;b.点燃酒精灯;c.熄灭酒精灯;d.停止通入氢气。其中,先通氢气后点燃酒精灯的目的是__。
②硬质粗玻璃管中发生的现象是_________;反应的化学方程式是_________。
③装置 A 中的玻璃管和其中物质在反应前后的质量差为 m1,装置 B 和其中物质在反应前后的质量差为m2,据此可计算出水中 H、O 元素的质量比为_____________(用含 m1、m2 的代数式表示)。实验时,该比值往往略大于1:8,原因可能是_____(填序号)。
A.氢气中含有水蒸气
B.装置A 中生成的铜又部分被氧化
C.空气中的水蒸气、二氧化碳等进入装置 B 中
D.有少量水蒸气液化残留在硬质玻璃管中
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将一小块银白色的金属钠放置在空气中会发生下列变化:
钠(Na)![]() 钠的氧化物
钠的氧化物![]() 氢氧化钠溶液
氢氧化钠溶液![]() 白色固体
白色固体
【提出问题】:常温下钠与氧气反应,产物有哪些?
【查阅资料】:钠的氧化物,除氧化钠(Na2O)外还有过氧化钠(Na2O2),氧化钠与过氧化钠都能与水发生反应,方程式如下:
Na2O+H2O=2NaOH;2Na2O2+2H2O=4NaOH+O2↑
【作出猜想】:常温下钠与氧气反应的产物.
猜想1:Na2O,
猜想2:Na2O2,
猜想3:
【实验探究一】:
实验操作 | 实验现象 | 实验结论 |
取少量钠的氧化物加入足量蒸馏水 | 猜想1正确 |
【继续探究】:钠在空气中放置一段时间得到白色固体的成分
【作出猜想】
猜想一:Na2CO3
猜想二:Na2CO3和NaOH
【实验探究二】:
实验操作 | 实验现象 | 实验结论 |
1.取少量白色固体加入足量 | 产生白色沉淀 | 白色固体成分为Na2CO3和NaOH |
2.过滤、取少量滤液加入 |
【实验反思】
(1)类比氧化铜与盐酸的反应,写出氧化钠与盐酸反应的化学方程式 。
(2)过氧化钠也能与盐酸反应,方程式为:2Na2O2+4HCl=4NaCl+2H2O+X,X的化学式为 。
(3)能与酸反应只生成盐和水的氧化物称为碱性氧化物,请判断Na2O2 碱性氧化物(填“是”或“不是”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com