
���� �������������е�HCl�������Ͷ�Ӧ�Ļ�ѧ����ʽ����̼��Ƶ���������������Ʒ��̼��Ƶ�����������
��� �⣺
��1����Һϡ���������ʵ��������䣮��ϡ�ͼ�ˮ������Ϊy��
36%��100g=��100g+y����10%
y=260g
��2����̼��Ƶ�����Ϊx��
CaCO3+2HCl=CaCl2+CO2��+H2O
100����73
x ��36.5g��10%
$\frac{100}{73}$=$\frac{x}{36.5g��10%}$
x=5g
��Ʒ��̼��Ƶ���������Ϊ��$\frac{5g}{6g}$��100%��83.3%
�𣺣�1������������Ϊ36%��Ũ����100g���Ƴ�����10%��ϡ���ᣬ�����ˮ������Ϊ 260g��
��2����Ʒ��̼��Ƶ���������Ϊ83.3%��
���� ���ݻ�ѧ����ʽ����ʱ����һҪ��ȷ��д��ѧ����ʽ���ڶ�Ҫʹ����ȷ�����ݣ������������Ҫ������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
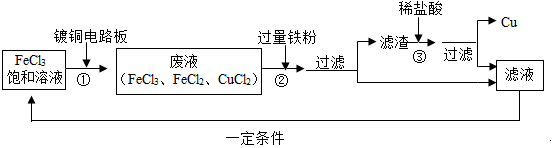
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 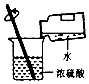 ϡ��Ũ���� | B�� | 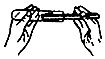 ȡ��̼���Ʒ�ĩ | C�� |  �ⶨ��Һ��pH | D�� | 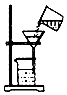 ��Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
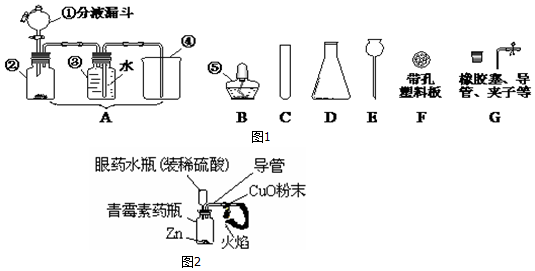
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
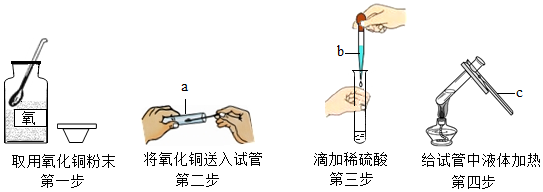
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
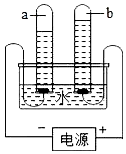 ���ˮ��ʵ��װ����ͼ��ʾ������ͼ�ش�
���ˮ��ʵ��װ����ͼ��ʾ������ͼ�ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��˿�ڿ�����ȼ��ʱ���������䣬�к�ɫ�������� | |
| B�� | �����ڿ�����ȼ�գ�ð���̣��к�ɫ�������� | |
| C�� | ʯ����������ȼ����ˮ�Ͷ�����̼���� | |
| D�� | ����ɫ����ͭ��Һ�еμ���ɫ����������Һ������ɫ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com