
·ÖĪö ĮņŌŚŃõĘųÖŠČ¼ÉÕÉś³É¶žŃõ»ÆĮņ£»
Į×ŌŚŃõĘųÖŠČ¼ÉÕÉś³ÉĪåŃõ»Æ¶žĮ×£»
Ģ¼ŌŚŃõĘųÖŠČ¼ÉÕÉś³É¶žŃõ»ÆĢ¼£»
ĢśŌŚŃõĘųÖŠČ¼ÉÕÉś³ÉĖÄŃõ»ÆČżĢś£®
½ā“š ½ā£ŗ¢ŁĮņČ¼ÉյĻÆѧ·½³ĢŹ½ĪŖ£ŗS+O2$\frac{\underline{\;µćČ¼\;}}{\;}$SO2£¬·“Ó¦ĻÖĻóŹĒ£ŗ¾ēĮŅČ¼ÉÕ£¬·¢³öĆ÷ĮĮµÄĄ¶×ĻÉ«»šŃę£¬·Å³öČČĮ棻
¢ŚĮ×Č¼ÉյĻÆѧ·½³ĢŹ½ĪŖ£ŗ4P+5O2$\frac{\underline{\;µćČ¼\;}}{\;}$2P2O5£¬·“Ó¦ĻÖĻóŹĒ£ŗ¾ēĮŅČ¼ÉÕ£¬·Å³öČČĮ棬²śÉś“óĮæ°×ŃĢ£»
¢ŪĢ¼Č¼ÉյĻÆѧ·½³ĢŹ½ĪŖ£ŗC+O2$\frac{\underline{\;µćČ¼\;}}{\;}$CO2£¬·“Ó¦ĻÖĻóŹĒ£ŗ¾ēĮŅČ¼ÉÕ£¬·¢³öŅ«ŃŪµÄ°×¹ā£¬·Å³öČČĮ棻
¢ÜĢśĖæČ¼ÉյĻÆѧ·½³ĢŹ½ĪŖ£ŗ3Fe+2O2$\frac{\underline{\;µćČ¼\;}}{\;}$Fe3O4£¬·“Ó¦ĻÖĻóŹĒ£ŗ¾ēĮŅČ¼ÉÕ£¬»šŠĒĖÄÉ䣬·Å³öČČĮæ£¬Éś³ÉŗŚÉ«¹ĢĢ壻
¢Ż2H2+O2$\stackrel{µćČ¼}{”ś}$2H2OøĆ»Æѧ·½³ĢŹ½ŗź¹Ū¶Į·ØĪŖ£ŗĒāĘųČ¼ÉÕÉś³ÉĖ®£¬Ī¢¹Ū¶Į·ØĪŖ£ŗĆæ2øöĒā·Ö×ÓŗĶ1øöŃõ·Ö×Ó·“Ӧɜ³É2øöĖ®·Ö×Ó£®
¹ŹĢī£ŗS+O2$\frac{\underline{\;µćČ¼\;}}{\;}$SO2£¬¾ēĮŅČ¼ÉÕ£¬·¢³öĆ÷ĮĮµÄĄ¶×ĻÉ«»šŃę£¬·Å³öČČĮ棻4P+5O2$\frac{\underline{\;µćČ¼\;}}{\;}$2P2O5£¬¾ēĮŅČ¼ÉÕ£¬·Å³öČČĮ棬²śÉś“óĮæ°×ŃĢ£»C+O2$\frac{\underline{\;µćČ¼\;}}{\;}$CO2£¬¾ēĮŅČ¼ÉÕ£¬·¢³öŅ«ŃŪµÄ°×¹ā£¬·Å³öČČĮ棻3Fe+2O2$\frac{\underline{\;µćČ¼\;}}{\;}$Fe3O4£¬¾ēĮŅČ¼ÉÕ£¬»šŠĒĖÄÉ䣬·Å³öČČĮæ£¬Éś³ÉŗŚÉ«¹ĢĢ壻ĒāĘųČ¼ÉÕÉś³ÉĖ®£¬Ćæ2øöĒā·Ö×ÓŗĶ1øöŃõ·Ö×Ó·“Ӧɜ³É2øöĖ®·Ö×Ó£®
µćĘĄ ŹéŠ“»Æѧ·½³ĢŹ½ŅŖ×¢ŅāĖIJ½£ŗŅ»ŹĒ·“Ó¦ĪļŗĶÉś³ÉĪļµÄ»ÆѧŹ½ŅŖÕżČ·£»¶žŹĒŅŖ×ńŃÖŹĮæŹŲŗć¶ØĀÉ£¬¼“ÅäĘ½£»ČżŹĒŅŖÓŠ±ŲŅŖµÄĢõ¼ž£»ĖÄŹĒæ“ŹĒ·ńŠčŅŖ”°”ü”±»ņ”°”ż”±£®


 ĒįĖÉæĪĢƵ„ŌŖ²āŹŌAB¾ķĻµĮŠ“š°ø
ĒįĖÉæĪĢƵ„ŌŖ²āŹŌAB¾ķĻµĮŠ“š°ø Š”Ģāæń×öĻµĮŠ“š°ø
Š”Ģāæń×öĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
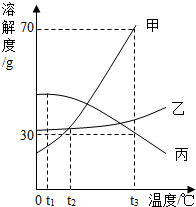 ČēĶ¼ĪŖ¼×”¢ŅŅ”¢±ūČżÖÖ¹ĢĢåĪļÖŹČܽā¶ČĒśĻߣ¬¾ŻĶ¼»Ų“š£ŗ
ČēĶ¼ĪŖ¼×”¢ŅŅ”¢±ūČżÖÖ¹ĢĢåĪļÖŹČܽā¶ČĒśĻߣ¬¾ŻĶ¼»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ĢāŗÅ | »Æѧ·½³ĢŹ½ | ĘĄ¼Ū | ·“Ó¦ĄąŠĶ |
| £Ø1£© | Mg+O2$\frac{\underline{\;µćČ¼\;}}{\;}$MgO2 | ¢ŁB | ¢Śb |
| £Ø2£© | 2H2O$\frac{\underline{\;µē½ā\;}}{\;}$H2+O2”ü | ¢ŪC | ¢Üa |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
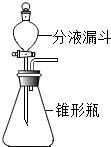 ŹµŃéŹŅÓĆ¹żŃõ»ÆĒāČÜŅŗŌŚ¶žŃõ»ÆĆĢ×÷“߻ƼĮµÄĢõ°éĻĀÖĘČ”ŃõĘų£®Ä³Ń§ÉśÉč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ£¬æÉŅŌĶعż·ÖŅŗĀ©¶·µÄ»īČūæŲÖĘŅŗĢåµÄµĪ¼ÓĖŁ¶Č£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ŹµŃéŹŅÓĆ¹żŃõ»ÆĒāČÜŅŗŌŚ¶žŃõ»ÆĆĢ×÷“߻ƼĮµÄĢõ°éĻĀÖĘČ”ŃõĘų£®Ä³Ń§ÉśÉč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ£¬æÉŅŌĶعż·ÖŅŗĀ©¶·µÄ»īČūæŲÖĘŅŗĢåµÄµĪ¼ÓĖŁ¶Č£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ij²¹øĘ¼ĮĖµĆ÷ŹéµÄ²æ·ÖŠÅĻ¢ČēĶ¼ĖłŹ¾£®Š”Ć÷¶ŌøĆ²¹øĘ¼ĮŹ®·ÖøŠŠĖȤ£¬Č”10ʬøĘʬ·ÅČė100gĻ”ŃĪĖįÖŠ£¬ÓŠŠ§³É·ÖøÕŗĆĶźČ«·“Ó¦£ØĘäĖū³É·Ö²»ÓėŃĪĖį·“Ó¦£©£¬Ź£Óą¹ĢĢåŗĶŅŗĢå×ÜÖŹĮæ±Č·“Ó¦Ē°¼õÉŁĮĖ2.2g£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCaCO3+2HClØTCaCl2+H2O+CO2”ü£®ĒėĶź³ÉĻĀĮŠĪŹĢā£ŗ
ij²¹øĘ¼ĮĖµĆ÷ŹéµÄ²æ·ÖŠÅĻ¢ČēĶ¼ĖłŹ¾£®Š”Ć÷¶ŌøĆ²¹øĘ¼ĮŹ®·ÖøŠŠĖȤ£¬Č”10ʬøĘʬ·ÅČė100gĻ”ŃĪĖįÖŠ£¬ÓŠŠ§³É·ÖøÕŗĆĶźČ«·“Ó¦£ØĘäĖū³É·Ö²»ÓėŃĪĖį·“Ó¦£©£¬Ź£Óą¹ĢĢåŗĶŅŗĢå×ÜÖŹĮæ±Č·“Ó¦Ē°¼õÉŁĮĖ2.2g£¬·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCaCO3+2HClØTCaCl2+H2O+CO2”ü£®ĒėĶź³ÉĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com