
【题目】下列是实验室中常见的几项化学实验基本操作,其中正确的是
A. 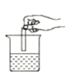 测溶液pH B.
测溶液pH B. 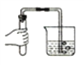 检查装置气密性
检查装置气密性
C. 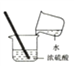 稀释浓硫酸 D.
稀释浓硫酸 D. ![]() 过滤
过滤
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示.下列叙述正确的是( )

A. 甲的溶解度大于乙的溶解度
B. t2℃时,用等质量的甲和乙固体配制饱和溶液,得到乙溶液的质量大于甲
C. 将甲、乙的饱和溶液从t1℃升温至t2℃,甲溶液中溶质的质量分数比乙大
D. 将甲和乙的饱和溶液从t2℃降温至t1℃,甲析出的晶体多
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组用以下装置探究炼铁原理。
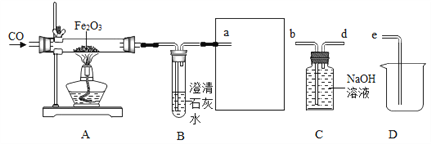
(1)加热氧化铁前要先通一会儿纯净的一氧化碳,其目的是_____;
(2)方框中连接的是装置C和D,导管接口的正确顺序为a→_____→_____→e。
(3)装置A玻璃管中观察到的实验现象为_____,发生反应的化学方程式为_____。为了确认反应进行情况,该小组甲、乙两位同学进行了如下讨论和实验。
甲同学认为:只要装置B中石灰水变浑浊,证明反应发生了。装置B中发生反应的化学方程式为_____。
乙同学取反应一段时间后装置A玻璃管中的剩余固体,冷却后,加入足量的稀盐酸,观察溶液由无色变为黄色,有关化学方程式为_____,该反应的基本反应类型为_____;同时还观察有气泡产生,有关化学方程式为_____。根据以上现象证明装置A中的氧化铁部分反应。
(4)装置B中澄清石灰水的作用是检验二氧化碳的产生,装置C中NaOH溶液的作用是_____,发生反应的化学方程式为_____。
(5)某钢铁公司用1000t含氧化铁80%的赤铁矿,理论上最多可炼得铁的质量为_____t。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,A~F是初中化学常见的物质,其中A是紫红色金属,B、E常温下均是气体,E、F都能用于灭火,C是人体胃液中含有的酸。图中“—”表示物质间能发生化学反应,“→”表示物质间的转化关系。请回答:
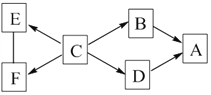
(1)A的一种用途是______________。
(2)B、E的化学式分别为______、______。
(3)D→A的化学方程式为______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(3分)向一定质量AgNO3。和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示。

(1)请写出a点所发生反应的化学方程式。
(2)e点所示的溶液中含有哪些溶质?
(3)d点表示的固体中含有哪些物质?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以FeSO4为原料制备铁黑颜料Fe3O4(其中Fe既有+2价,也有+3价)的过程如下:
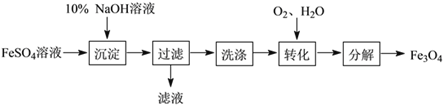
“转化”过程的反应为:4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3。“分解”过程发生的反应为:2Fe(OH)3 + Fe(OH)2 = Fe3O4+4H2O。若原料中含FeSO4 9.12 t,下列说法正确的是
A. 理论上与FeSO4反应的NaOH溶液的质量为4.8 t
B. 理论上“转化”过程参与反应的O2的质量为320 kg
C. 该方法理论上最终可以获得Fe3O4的质量为4.64 t
D. 若“转化”过程参与反应的O2过量,则最终所得固体的质量偏小
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图.
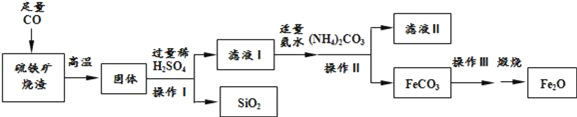
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器玻璃棒、___、烧杯等.
(2)写出通入CO后所发生反应的化学方程式______________________(只要写一个).
(3)滤液Ⅰ的颜色是___,该溶液的pH__7 (填>、=、<).
(4)若在滤液Ⅰ中不先加入氨水,而是直接加入(NH4)2CO3,则开始出现的现象是___.
(5)滤液Ⅱ中可回收的产品的化学式是______.
(6)为了提高得到的Fe2O3的纯度,操作Ⅲ应该是______.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化氯(ClO2)可用于自来水消毒.以粗盐为原料生产ClO2的工艺主要包括:①粗盐精制;②特殊条件下电解NaCl溶液制NaClO3;③ClO2的制取.工艺流程如图,其中反应Ⅲ制取ClO2的化学方程式为2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O。
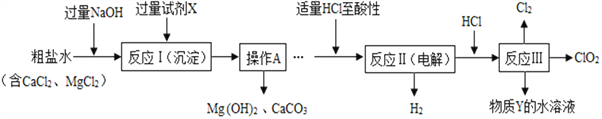
(1)试剂X是___________(填化学式)。
(2)操作A中用到玻璃棒的作用是_____________。
(3)加入适量HCl至酸性过程中,发生的中和反应的化学方程式是___________。
(4)写出反应II的化学方程式___________________________。
(5)该流程中可以循环利用的物质是水和_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组为测定某赤铁矿中氧化铁的含量,取10 g赤铁矿(主要成分为Fe2O3,假设其中的杂质不溶于水,也不与稀硫酸反应)置于烧杯中,加入足量的稀硫酸,烧杯中剩余固体的质量随反应时间的变化曲线如图所示。
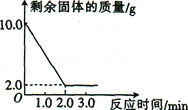
请计算:(1)Fe2O3中铁元素的质量分数为_______ 。
(2)反应中消耗H2SO4的质量_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com