
| 实验 | 现象 | 化学方程式 |
| 铝丝插入硫酸铜溶液中 | ||
| 铜丝插入硝酸银溶液中 | ||
| 铜丝插入硫酸铝溶液中 |
分析 根据将铝丝浸入硫酸铜溶液中、铜丝浸入硝酸银溶液中、铜丝浸入硫酸铝溶液中的反应现象,判断能否发生反应,进而可确定三种金属活动性由强到弱的顺序.
解答 解:
将铝丝浸入硫酸铜溶液中,铝丝表面有红色物质析出,溶液变为无色,铝与硫酸铜溶液反应生成硫酸铝溶液和铜,说明铝的金属活动性比铜强,即铝>铜,反应的化学方程式为:2Al+3CuSO4=3Cu+Al2(SO4)3.
将铜丝浸入硝酸银溶液中,铜丝表面有银白色物质析出,溶液变为蓝色,铜与硝酸银溶液反应生成硝酸铜溶液和银,说明铜的金属活动性比银强,即铜>银,反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2.
将铜丝浸入硫酸铝溶液中,无明显变化,说明铜的金属活动性比铝弱,即铝>铜.
铝>铜,铜>银,铝>铜,则三种金属的活动性顺序为铝>铜>银.
故答案为:
| 实验步骤 | 现象 | 反应的化学方程式 |
| 将铝丝浸入硫酸铜溶液中 | 铝丝表面有红色物质析出,溶液变为无色 | 2Al+3CuSO4=3Cu+Al2(SO4)3 |
| 将铜丝浸入硝酸银溶液中 | 铜丝表面有银白色物质析出,溶液变为蓝色 | Cu+2AgNO3=2Ag+Cu(NO3)2 |
| 将铜丝浸入硫酸铝溶液中 | 无明显现象 | / |
点评 本题难度不大,考查了金属活动性顺序的应用,掌握金属活动性顺序并能灵活运用是正确解答此类题的关键所在.


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:初中化学 来源: 题型:选择题
| A. | 变大 | B. | 不变 | C. | 变小 | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
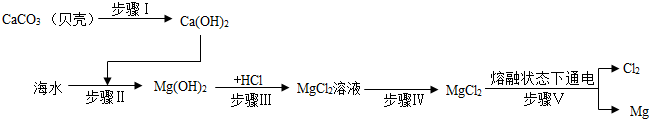
| A. | 步骤Ⅰ通过一步反应即可实现 | |
| B. | 步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁 | |
| C. | 步骤Ⅴ中化学能转化为电能 | |
| D. | 在此流程中涉及的基本反应类型有4种 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 |
| A | FeSO4溶液(CuSO4) | 过量铁粉 |
| B | CO2气体(CO) | 氢氧化钠溶液 |
| C | CaO固体(CaCO3) | 稀盐酸 |
| D | NaCl溶液(Na2CO3) | 过量氯化钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 绿原酸属于有机高分子 | |
| B. | 绿原酸由碳、氧三种元素质量比为16:9 | |
| C. | 绿原酸的相对分子质量为354 | |
| D. | 绿原酸中氧元素的质量分数最大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com