下列有关叙述中,正确的是( )
A.20℃,100g水中能溶解36gNaCl,所以20℃时NaCl的溶解度是36g
B.NaCl饱和溶液中加入大量水后,溶液中溶质的质量减少了
C.饱和溶液降温后,都有溶质结晶析出
D.在同一温度下,NaCl的饱和溶液一定比不饱和溶液浓
【答案】分析:A、根据溶解度概念解答;
B、根据溶液加水稀释后各量的变化确定;
C、根据结晶的方法解答;
D、根据饱和溶液、不饱和溶液与溶液浓稀之间的关系解答.
解答:解:A、溶解度是在一定温度下,100克溶剂中达到饱和状态时所溶解的这种物质的质量,A中没说饱和,故错误;
B、NaCl饱和溶液中加入大量水后,溶液中溶质的质量不变,溶剂、溶液质量增多,说法错误;
C、饱和溶液降温后不一定都有溶质结晶析出,对于溶解度随温度升高而减小的物质来说就没有晶体析出,如氢氧化钙,说法错误;
D、在同一温度下,某物质饱和溶液的浓度达到最大值,NaCl的饱和溶液一定比不饱和溶液浓,说法正确.
故选D
点评:溶解度四要素缺一不可:一定温度、100g溶剂、饱和状态、溶质质量单位克.



 阅读快车系列答案
阅读快车系列答案
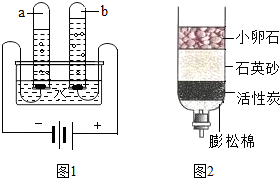 2012年3月22日是第二十届“世界水日”.水与人类的生活和生产密切相关.
2012年3月22日是第二十届“世界水日”.水与人类的生活和生产密切相关.