
| A. | MnO2 | B. | Ca(OH)2 | C. | 稀盐酸 | D. | NaCl |
分析 根题题意,过碳酸钠(2Na2CO3•3H2O2)晶体具有碳酸钠和过氧化氢的双重性质,据此结合碳酸钠与过氧化氢的化学性质,进行分析判断.
解答 解:由题意,过碳酸钠(2Na2CO3•3H2O2)晶体具有碳酸钠和过氧化氢的双重性质,凡是与双氧水或碳酸钠反应的物质均能与过碳酸钠反应使之变质失效.
A、过氧化氢在二氧化锰的催化作用下生成水和氧气,会导致过碳酸钠变质失效,故选项错误.
B、碳酸钠能与Ca(OH)2反应生成碳酸钙沉淀和氢氧化钠,会导致过碳酸钠变质失效,故选项错误.
C、碳酸钠能与稀盐酸反应生成氯化钠、水和二氧化碳,会导致过碳酸钠变质失效,故选项错误.
D、氯化钠不与碳酸钠、过氧化氢反应,不会导致过碳酸钠变质失效,故选项正确.
故选:D.
点评 本题难度不大,理解凡是与双氧水或碳酸钠反应的物质均能使过碳酸钠变质,掌握碳酸钠与双氧水的化学性质是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
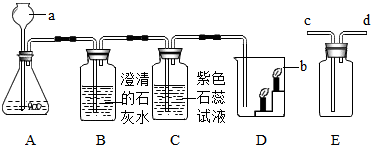
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
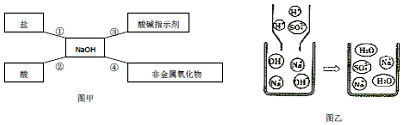
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
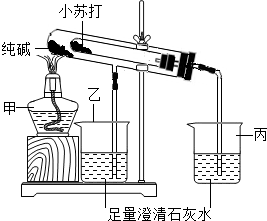 某化学兴趣小组设计了如图所示的装置,对纯碱(Na2CO3)和小苏打(NaHCO3)两种固体进行实验探究.
某化学兴趣小组设计了如图所示的装置,对纯碱(Na2CO3)和小苏打(NaHCO3)两种固体进行实验探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2CO3 | B. | Ba(OH)2 | C. | H2SO4 | D. | NaHCO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲车间的污水中可能含有Ba2+ | B. | 乙车间的污水中可能含有Na+ | ||
| C. | 乙车间的污水中一定含有Fe3+ | D. | 甲车间的污水中不可能含有SO42- |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
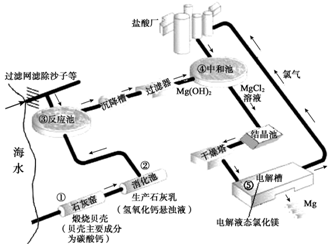
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com