
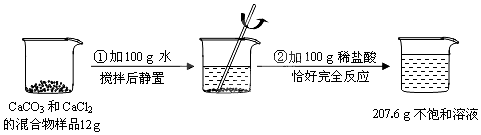
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算碳酸钙和生成氯化钙的质量,进而求算对应的质量分数.
解答 解:
根据质量守恒定律,二氧化碳的质量为:12g+100g+100g-207.6g=4.4g;
CaCO3中钙、碳、氧元素的质量比为40:12:(16×3)=10:3:12
设该石灰石样品中碳酸钙的质量为x,生成氯化钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
$\frac{100}{x}$=$\frac{111}{y}$=$\frac{44}{4.4g}$
x=10g
y=11.1g
则原混合物中氯化钙的质量为12g-10g=2g
所得溶液中氯化钙的质量为2g+11.1g=13.1g
反应后的CaCl2 不饱和溶液中溶质的质量分数为$\frac{13.1g}{207.6g}$×100%≈6.3%
答:(1)实验过程中产生的CO2气体的质量为 4.4 g
(2)CaCO3中钙、碳、氧元素的质量比 10:3:12.(本空回答成其他顺序也可以)
(3)反应后的CaCl2 不饱和溶液中溶质的质量分数为6.3%
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:初中化学 来源: 题型:填空题
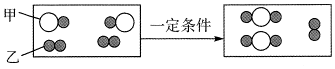

 ”聚集成的物质可能(填“可能”或“不可能”)是氧化物.
”聚集成的物质可能(填“可能”或“不可能”)是氧化物.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 回收利用废旧金属 | B. | 用硝酸工厂废水浇灌菜地 | ||
| C. | 将取出的剩余药品放回原瓶 | D. | 吃经高温蒸煮后的霉变大米 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
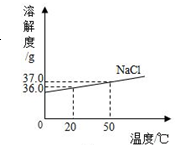 2017年1月《科学报告》一篇文章称,只需在普通口罩上添加氯化钠涂层,就能将其转化为“特效口罩”.口罩使用过程中,涂层中的氯化钠在溶解于病毒自身携带的水中,形成溶液,杀死病毒;杀死病毒后,水分蒸发,氯化钠会再次析出.右图为氯化钠的溶解度曲线图.
2017年1月《科学报告》一篇文章称,只需在普通口罩上添加氯化钠涂层,就能将其转化为“特效口罩”.口罩使用过程中,涂层中的氯化钠在溶解于病毒自身携带的水中,形成溶液,杀死病毒;杀死病毒后,水分蒸发,氯化钠会再次析出.右图为氯化钠的溶解度曲线图.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
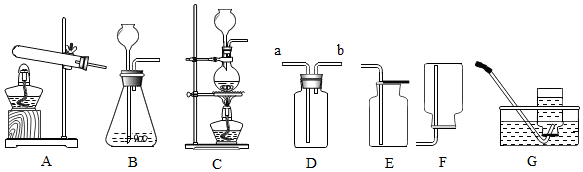
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com