
【题目】酸、碱、盐在生产和生活中有广泛的应用。
(1)焙制糕点所用发酵粉中含有碳酸氢钠,其俗名为______(填字母代号)。
a纯碱
b烧碱
c苏打
d小苏打
(2)如图1是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。
①根据图示判断,该实验是将______(填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液中。
②滴入溶液体积为V2mL时,溶液中的溶质为_______。
(3)为除去粗盐水中的可溶性杂质MgSO4、CaCl2,某化学小组设计了如图2方案:
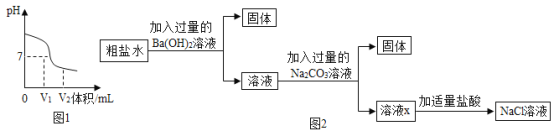
①过滤用到的玻璃仪器有烧杯、玻璃棒和______。
②写出加入Ba (OH) 2溶液时反应的化学方程式____。(提示:微溶物不形成沉淀)
③溶液X中含有哪些杂质?______。
【答案】d 硫酸 硫酸和硫酸钠 漏斗 ![]() 碳酸钠和氢氧化钠
碳酸钠和氢氧化钠
【解析】
氢氧化钡和碳酸钠反应生成碳酸钡和氢氧化钠,稀硫酸和氢氧化钠反应生成硫酸钠和水,氢氧化钡和硫酸镁反应生成氢氧化镁和硫酸钡。
(1)焙制糕点所用发酵粉中含有碳酸氢钠,其俗名为小苏打,故选d。
(2)①开始pH值大于7,溶液显碱性,滴加药品的过程中,pH在变小,最终小于7,故该实验是将硫酸滴加到另一种溶液中。
②滴入溶液体积为V2mL时,此时pH小于7,说明硫酸过量,稀硫酸和氢氧化钠反应生成硫酸钠和水,故溶液中的溶质为生成的硫酸钠和过量的硫酸。
(3)①过滤用到的玻璃仪器有烧杯、玻璃棒和漏斗。
②加入Ba (OH) 2溶液和硫酸镁反应生成硫酸钡和氢氧化镁沉淀,对应的化学方程式为![]() 。
。
③氢氧化钡和碳酸钠反应生成碳酸钡和氢氧化钠,加入过量的碳酸钠,故溶液X含有的溶质除氯化钠外还有碳酸钠和氢氧化钠。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:初中化学 来源: 题型:
【题目】实验小组做了如下图所示实验。
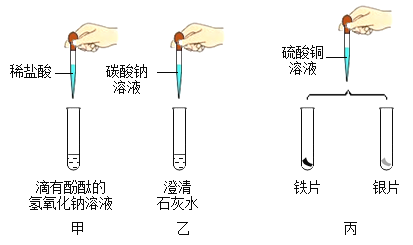
(1)能证明甲中发生反应的现象是_____。
(2)乙中可观察到的现象是_____,发生反应的化学方程式为_____。
(3)丙中观察到的现象为_____, 由该实验现象推断,三种金属活动性由强到弱为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定量的硝酸铜、硝酸亚铁的混合溶液中加入 2.4g 镁粉,充分反应后过滤、洗涤、 干燥,称得固体 6g。则下列分析正确的是( )
A.滤液中一定不含有硝酸铜B.滤液中一定含有硝酸亚铁
C.滤出的固体中可能有铜无铁D.滤出的固体中可能只有铜和镁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属是一种非常重要的资源,在生产、生活中有着广泛的用途.
(1)人类每年从自然界提取大量的金属,其中提取量最大的是铁.用赤铁矿和一氧化碳炼铁的化学方程式为_____.
(2)央视315晚会曝光某品牌汽车厂为了节约成本,采用价格相对便宜的普通钢板代替防腐性能较好的镀锌板,造成钢板生锈,给车主带来极大安全隐患.普通钢板在空气中锈蚀,实际上是铁跟空气中的_____共同作用的结果.
(3)请写出工业上用稀硫酸除铁锈的化学反应方程式_____.
(4)亮亮同学用稀盐酸和另一种溶液,验证了Mg、Fe、Cu、Ag四种金属的活动性顺序是依次减弱的.请问亮亮所用的另一种溶液是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A-E为初中化学常见物质,其中A是常见的建筑材料,A、B、C、D分别为不同物质类别。请回答相关问题:(图中的短线表示物质之间能发生化学反应,箭头表示一种物质转化为另一种物质)

(1)B的化学式_______。
(2)写出E![]() D的化学方程式:_______。
D的化学方程式:_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
物质 | A | B | C | D |
反应前质量 |
|
|
|
|
反应后质量 | 待测 |
| 0 |
|
下列说法正确的是![]()
A. 物质C一定是反应物,物质D可能是单质
B. 反应后密闭容器中A的质量为![]()
C. 反应过程中,物质B和物质D变化的质量比为87:36
D. 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】去年入秋以来,我市干旱少雨.在农业生产上,用0.1%的氯化钙溶液以1:1浸种5~6小时后播种,可以提高种子在干旱条件下的出芽率.
①欲配制20kg 0.1%的氯化钙溶液浸种,需要氯化钙_____kg.
②以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产氯化钙的主要流程如下.
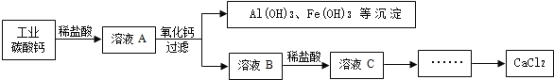
碳酸钙与稀盐酸反应的化学方程式为_____,向溶液B中加入稀盐酸的作用是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁是当今世界上应用最广泛的金属
(1)铁与潮湿的空气接触易生锈。对铁锈蚀的影响因素进一步探究如下:
组别 | 1 | 2 | 3 | 4 | 5 |
图示 |
|
|
|
|
|
生锈时间 | 8min | 较长时间不生锈 | 5min | 3min | 1min |
通过上述第_____组对比实验能证明温度越高,铁钉生锈的速率越快。利用上述实验,还可得出的结论是_____。
(2)实验室以Fe2O3为原料模拟炼铁的化学方程式为_____。
(3)以Fe2O3为原料制备合成氨工业生产中所需的a-Fe催化剂(主要成分FeO、Fe2O3),原理为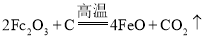 。当催化剂中FeO与Fe2O3的质量之比为9:20时,其催化活性最高。此时Fe2O3的转化率为_____( 精确到1%)。
。当催化剂中FeO与Fe2O3的质量之比为9:20时,其催化活性最高。此时Fe2O3的转化率为_____( 精确到1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示的实验中,得出的结果不正确的是
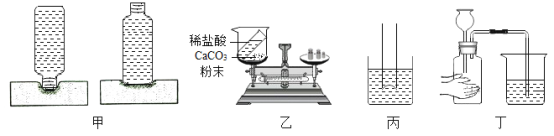
A.甲:同一瓶子放法不同,海绵凹陷程度不同,说明压力的作用效果与受力面积有关
B.乙:反应前后天平不平衡,说明碳酸钙和稀盐酸反应遵循质量守恒定律
C.丙:玻璃管扎有薄膜的一端放入水中,薄膜向上凸起,说明液体内部有向上的压强
D.丁:烧杯中导管口无气泡冒出,说明装置漏气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com