
| 13 Al 铝 26.98 | 14 Si 硅 28.09 |
| 类铝 | 类硅 |
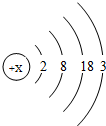 ,常见化合价为+3.
,常见化合价为+3.分析 (1)根据在原子中,质子数=核外电子数,进行解答;离原子核最远的是最外层,依据原子结构示意图即可解答;
(2)物质的色、味、态、熔、沸点、密度、硬度、水溶性等属于物理性质;物质的化学性质包括可燃性、氧化性、还原性、稳定性、酸性、碱性、热解性等,通常描述的语句中有能、可以、可等字眼儿进行解答;
(3)由于镓常见化合价为+3,硫酸根的根价为-2,利用十字交叉法即可写出化学式.
解答 解:(1)根据在原子中,质子数=核外电子数,由原子结构示意图可知镓元素原子的质子数为:31;
最外层电子数为:3;
(2)根据物质的色、味、态、熔、沸点、密度、硬度、水溶性等属于物理性质,从题中可知
镓的物理性质为:镓是银白色金属,密度为5.94g•cm-3;
根据镓能与沸水剧烈反应生成氢气和氢氧化镓反应化学方程式为:2Ga+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Ga(OH)3+3H2↑;
根据目前金属镓广泛用于制造半导体材料,可知镓的用途为:制造半导体材料;
故答案为:银白色金属,密度为5.94g•cm-3; 2Ga+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Ga(OH)3+3H2↑; 制造半导体材料;
(3)由于镓常见化合价为+3,硫酸根的根价为-2,利用十字交叉法写出硫酸镓的化学式为:Ga2(SO4)3;
故答案为:Ga2(SO4)3 .
答案:
(1)31 3
(2)银白色金属,密度为5.94g•cm-3;2Ga+6H2O$\frac{\underline{\;\;△\;\;}}{\;}$2Ga(OH)3+3H2↑; 制造半导体材料
(3)Ga2(SO4)3
点评 本题考查学生根据题中所给的信息及所学知识进行分析解题的能力,注意书写化学方程式的写配标等.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用pH试纸不能区分肥皂水和食醋 | |
| B. | 用灼烧的方法能区别棉花和羊毛 | |
| C. | 发生复分解反应产物中有水或气体或沉淀产生 | |
| D. | 用饱和(NH4)2SO4溶液能区分食盐水和蛋白质溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

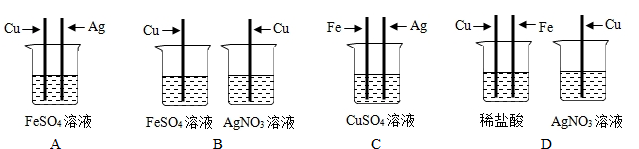
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SO4 NaNO3 KOH | B. | FeCl3 BaCl2 Mg(NO3)2 | ||
| C. | Na2SO4 KCl NaCl | D. | KNO3 K2SO4 BaCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
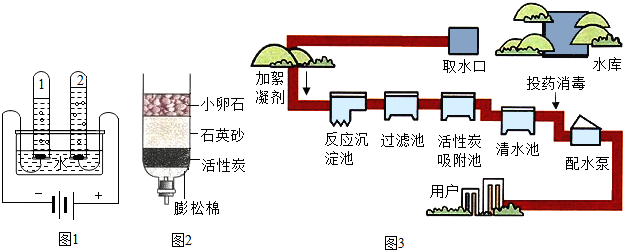
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
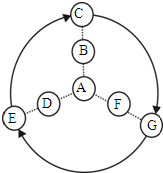 如图表示初中常见几种不同化合物之间的关系,图中虚线两端的化合物可以转化或相互反应,箭头表示物质间存在转化关系;反应条件、部分反应物和生成物已略去.请根据以下每小题的具体情况进行解答.
如图表示初中常见几种不同化合物之间的关系,图中虚线两端的化合物可以转化或相互反应,箭头表示物质间存在转化关系;反应条件、部分反应物和生成物已略去.请根据以下每小题的具体情况进行解答.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com