
| A. |  | B. |  | C. | 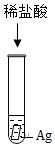 | D. |  |
科目:初中化学 来源: 题型:选择题
| 甲 | 乙 | 丙 |  |
 |  |  |
| A. | 物质X是氧化物 | |
| B. | 物质X的质量为2.8g | |
| C. | 物质甲的化学式是NH3 | |
| D. | 该反应化学方程式中物质X与O2的化学计量之比为2:3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 盐-食盐-NaCl | B. | 碱-烧碱-KOH | ||
| C. | 化肥-复合肥-K2CO3 | D. | 冰-干冰-H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 空烧杯的质量 | 实验前样品和烧杯的总质量 | 加入稀盐酸的质量 | 反应后烧杯和剩余物的总质量 |
| 100.2g | 112.2g | 50g | 157.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO2:“2”表示一个二氧化碳分子含有两个氧原子 | |
| B. | 2Fe:“2”表示两个铁元素 | |
| C. | $\stackrel{+2}{Mg}$:“+2”表示镁元素的化合价为+2价 | |
| D. | 2NH4+:“2”表示两个铵根离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加Na2CO3溶液 | 产生大量的气泡 | 该溶液是稀盐酸,反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
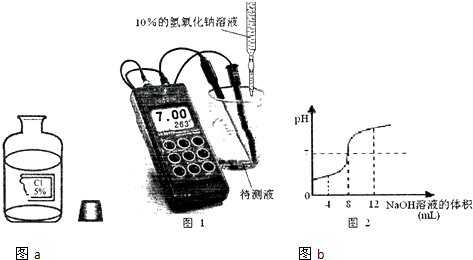
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
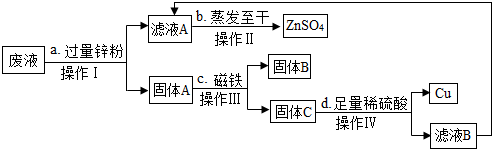
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com