
���� ��1������Ũ����������Լ�����ʽ��д����������
��2������Ũ����������Լ�ϡ��Ũ����ķ�����������
��3�������������Ƶ��׳ơ��ܽ�������仯�Լ����ȵIJⶨ������������
��4������̼�����ƵĻ�ѧ������������
��� �⣺��1��Ũ����ƿ�ڳ��ְ�������ΪŨ������лӷ��ԣ��������Ҫ�ɷ����������������ᷴӦ�����Ȼ�����ˮ����Ӧ�Ļ�ѧ����ʽ�ǣ�Fe2O3+6HCl�T2FeCl3+3H2O���÷�Ӧ�����ֻ�����������ɷ����������µĻ�����ķ�Ӧ�����ڸ��ֽⷴӦ������ӷ���Fe2O3+6HCl�T2FeCl3+3H2O�����ֽ⣻
��2��Ũ���������ˮ�ԣ��������������ϡ��Ũ����ʱ��Ҫ����Ũ������������ʣ��ܶȱ�ˮ��������ˮ������ˮʱ�ų��������ȣ������ˮ����Ũ�����У�ˮ�ḡ�����棬�ų���������ʹˮ���ڣ��Ӷ����Һ�ηɽ��������¹ʷ���������ϡ��Ũ����ʱҪ��Ũ���ᵹ��ˮ�У������Ͻ��裬ʹ����������ɢ����������Ũ���Ỻ����������ע��ˮ�У�
��3�����������׳ƻ��ռ�����ƣ�����ˮʱ��ų��������ȣ��ⶨ��Һ�����ȿ���pH��ֽ������ռ�ų���pH��ֽ��
��4��̼�����ƵĻ�ѧʽΪNaHCO3��̼�����ƺ����ᷴӦ�����������Ȼ��ơ�ˮ��������̼�����Է���ʽ�ǣ�NaHCO3+HCl=NaCl+H2O+CO2�������NaHCO3��NaHCO3+HCl=NaCl+H2O+CO2����
���� ���ճ�������ε����ơ��׳ơ���������;�ǽ���Ĺؼ����ѶȲ���


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 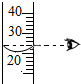 Һ����� | B�� |  �μ�Һ�� | C�� |  ��ҩƷ��ζ | D�� | 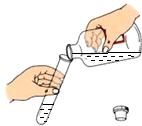 �㵹Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{1}{6.02��1{0}^{23}}$mL | B�� | $\frac{18}{6.02��1{0}^{23}}$ mL | ||
| C�� | $\frac{1}{18}$mL | D�� | $\frac{1}{18��6.02��1{0}^{23}}$mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
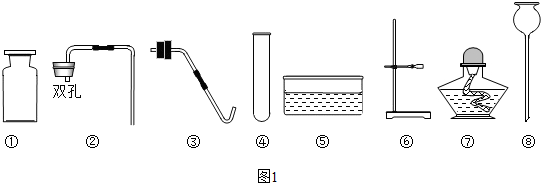
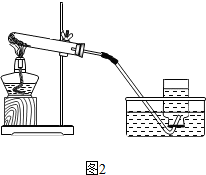
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
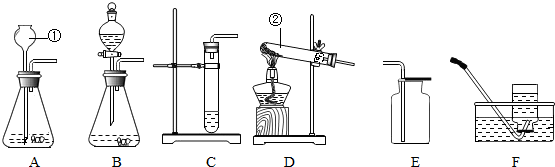
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com