
| A. | ①②③ | B. | ①②③④ | C. | ①③ | D. | ①②③⑤ |
分析 根据加热制取氧气,就是给试管中的固体加热,造成试管破裂的原因一般有:加热时试管外壁有水、用酒精灯的焰心加热、加热时没有预热、加热时试管口没有略向下倾斜、先撤了酒精灯,后移出导管等进行解答.
解答 解:根据给试管中的固体加热的注意事项,造成试管破裂的原因一般有:①没有给试管均匀预热;②试管外壁有水;③加热时试管口没有略向下倾斜,致使药品中含的水分在管口形成水滴倒流致使热的试管破裂;⑤加热时试管与灯芯接触;⑥先撤了酒精灯,后移出导管致使试管内温度降低,气压减小,冷水倒吸,使试管炸裂.没有加入催化剂二氧化锰,收集完氧气后,先将导管移出水面,再熄灭酒精灯,试管口没有略向上倾斜不会造成试管破裂.
答案:C.
点评 掌握实验室制取氧气的操作步骤和注意事项;了解给试管里的固体加热的方法是正确解答此题的依据.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:填空题
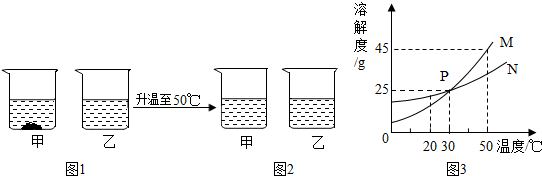
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酒精燃烧,汽油挥发,蜡烛变形 | |
| B. | 植物腐烂,钢铁生锈,牛奶变质 | |
| C. | 绿色植物的光合作用,铁铸成钢,蜡烛加热熔化 | |
| D. | 葡萄酿酒,水分蒸发,金属导电 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 U形管中是滴有紫色石蕊试液的蒸馏水,向左、右两管中分别同时滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示).下列说法正确的是( )
U形管中是滴有紫色石蕊试液的蒸馏水,向左、右两管中分别同时滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示).下列说法正确的是( )| A. | 开始时左边溶液呈蓝色,右边溶液呈红色 | |
| B. | 开始时左边溶液呈红色,右边溶液呈无色 | |
| C. | 充分反应后U型管内的溶液可能呈无色 | |
| D. | 充分反应后U型管内的溶液一定呈紫色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com