
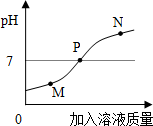
 在用稀HCl和NaOH溶液进行中和反应的实验时,溶液的pH变化曲线如图所示:
在用稀HCl和NaOH溶液进行中和反应的实验时,溶液的pH变化曲线如图所示:分析 (1)根据反应物盐酸和氢氧化钠中和生成水和氯化钠的过程,依照书写规则书写化学反应方程式.
(2)根据图象中pH值的变化是从小于7逐渐的增大到大于7,可以分析确定操作的过程;
(3)当反应进行到N点时,溶液呈碱性解答.
解答 解:
(1)该题是氢氧化钠和盐酸发生中和反应生成氯化钠和水的过程,故答案为:NaOH+HCl=NaCl+H2O.
(2)由图象可知,pH值是从小于7 逐渐的增大到7然后在大于7,可知原溶液是酸性的,然后不断的加碱,使PH升高,故答案为:①;
(3)当反应进行到N点时,溶液呈碱性,溶液中的溶质有NaCl; NaOH.
答案:(1)HCl+NaOH=NaCl+H2O;(2)①;(3)NaCl; NaOH.
点评 本题主要考查了从图象的角度对中和反应的正确理解,要学会这种数形结合的思想.


 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A、物质鉴别 | B、认识物质俗名 |
| 氢氧化钠固体和碳酸钙--加水,用手触摸试管 硬水和软水--用肥皂水,观察现象 | 氢氧化钙--熟石灰 氢氧化钠--火碱 |
| C、安全知识 | D、物质的微粒构成与宏观组成 |
| 电器着火--切断电源,再用二氧化碳灭火器灭火 液化气泄漏--先关闭阀门,再打开门窗通风 | 水--由氢原子和氧原子构成 氯化钠--由钠离子和氯离子构成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | M | N | P | Q |
| 反应前质量/g | 20 | 2 | 1 | 37 |
| 反应后质量/g | X | 32 | 1 | 12 |
| A. | 物质P可能是该反应的催化剂 | B. | X的值为15 | ||
| C. | 反应中N、Q的质量比为8:3 | D. | 该反应的基本类型为化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 木炭疏松多孔,所以具有吸附性 | |
| B. | 汽油具有乳化作用,所以可用于清除油污 | |
| C. | 氢氧化钠显碱性,所以可用于改良酸性土壤 | |
| D. | 二氧化碳的水溶液显酸性,所以可用于制作汽水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 序号 | KClO3的质量 | 其他物质的质量 | 温度 | 氧气的体积 | 反应所需时间 |
| ① | 2.0g | 330℃ | 100mL | t1 | |
| ② | 2.0g | CuO 0.5g | 330℃ | 100mL | t2 |
| ③ | 2.0g | MnO2 0.5g | 330℃ | 100mL | t3 |
| ④ | 2.0g | MnO20.5 g | 380℃ | 100mL | t4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com