
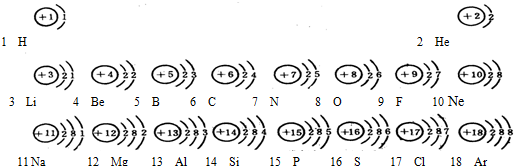
分析 (1)根据原子序数熟记前20号元素名称;在化学反应中,根据元素原子的最外层电子多少判定得失电子数目,推测化合价,书写化学式.
(2)根据元素周期律及图表中的信息进行分析解答.
解答 解:(1)原子序数为16的元素是硫元素,其原子结构最外层为6个电子,在化学反应中易得到2个电子形成带两个单位负电荷的硫离子;原子序数为11的元素为钠元素,属于金属元素,钠原子最外层为1个电子,在化学反应中易失去最外层的一个电子形成带一个单位正电荷的钠离子,钠元素与硫元素组成的化合物的化学式为Na2S;故填:硫;S2-;金属;Na2S;
(2)根据原子结构示意图的变化规律可知:电子层数等于周期数;同一周期中最外层电子数由1-8依次排列;同一纵行,原子最外层电子数相同,故答案为:电子层数等于周期数或同一周期中最外层电子数由1-8依次排列或同一纵行,原子最外层电子数相同.
点评 本题考查学生对元素周期律和元素的性质与最外层电子数的关系的理解与掌握,不能在解题中灵活应用.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
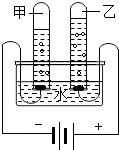 用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )
用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )| A. | ①②③④ | B. | ①② | C. | ②③ | D. | ①②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3 不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| a.取少量该溶液于一支试管中,加入足量的氯化钙溶液 | 有白色沉淀生成 | 该氢氧化钠溶液已变质 |
| b.将步骤a所得的液体过滤,取滤液于另一支试管中,滴加无色酚酞试液 | 酚酞试液变红 | 该氢氧化钠溶液已部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
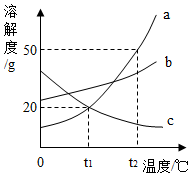 如图是三种固体物质的溶解度曲线.
如图是三种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.化学与健康 | B.化学与生活 |
| ①食用鲜黄瓜-可大量补钙 ②人体缺铁-易患贫血病 | ①减轻车内异味-开窗通风 ②防止食品受潮-用氧化钙做干燥剂 |
| C.化学与安全 | D.化学与环境 |
| ①重金属盐中毒-喝鲜牛奶解毒 ②煤气泄漏-关闭阀门,严禁烟火 | ①使用乙醇汽油-减少空气污染 ②合理使用农药、化肥-减少水污染 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com