
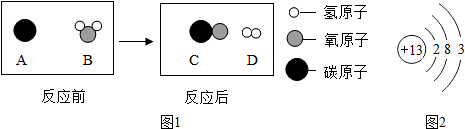
分析 Ⅰ、(1)煤、石油和天然气属于化石燃料,甲烷完全燃烧时能生成水和二氧化碳;
(2)①根据反应的微观示意图,分析反应的特点.判断反应的类型;
②根据反应的微观示意图及质量守恒定律分析反应生成物的分子个数比;
(3)根据反应物、生成物以及质量守恒定律写出化学方程式即可;
Ⅱ、(1)依据原子结构示意图的意义以及核外电子的得失规律和铝的有关性质分析解答;
(2)根据物质化学式的书写规则正确书写物质的化学式;
(3)若要验证三种金属的活动性,如果只用一种溶液,就要选择活动性居中的金属的盐溶液.氢氧化钠和硫化氢反应生成硫化钠和水;
根据反应物、生成物的种类可以判断反应类型;
(4)铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果.
解答 解:Ⅰ、(1)化石燃料包括天然气、煤和石油;天然气的主要成分是甲烷,甲烷在空气中完全燃烧的化学方程式是:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
故填:天然气;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)①由反应的微观示意图可知,该反应由一种单质和化合物反应,生成了另一种单质和另一种化合物,属于置换反应.
②由反应的微观示意图及质量守恒定律可知,该图示中一个碳原子与一个水分子反应,生成了一个易氧化碳分子和一个氢分子,所以,该反应生成物的分子个数比为1:1.
故填:①置换反应;②1:1.
NH3燃烧生成物是水和氮气(根据质量守恒定律:反应前后元素的种类不变,可以确定生成的气体是氮气),故化学方程式为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2;故填:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+2N2;
Ⅱ、(1)A、根据原子结构示意图的特点可知:铝的核内质子数为13,故A正确;
B、根据金属铝的性质可知:铝具有较好延展性和的导电性,所以可以用铝制作导线;故B正确;
C、依据地壳中元素的含有情况可知,铝是地壳中含量最多的金属元素,而含量最多的元素是氧;故C正确;
D、根据原子的核外电子在化学反应中的规律特点可知:铝的最外层电子数是3,且在化学反应中易失掉3个电子而达到稳定结构,故D错误;
故填:D
(2)铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,氧化铝是由显+3价的铝元素和显-2价的氧元素组成的,根据化合价原则,其化学式可表示为:Al2O3.
故填:Al2O3;
(3)验证三种金属的活动性,如果只用一种溶液,就要选择活动性居中的金属的盐溶液,所以,在硫酸铝溶液、硫酸亚铁溶液、硫酸铜溶液中应选用硫酸亚铁溶液.
故填:B;
(4)钢铁生锈实际是铁与空气中的氧气、水发生化学反应,所以在钢铁表面涂油、刷漆等,能防止钢铁生锈;
故填:氧气和水.
点评 本题主要考查了化石燃料的种类,煤的利用、反应的微观示意图,属于基础的知识,难度不大.根据已有的知识即可解答.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 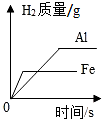 等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应 | |
| B. |  表示水通电分解产生的气体质量与反应时间的关系 | |
| C. | 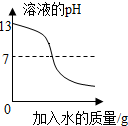 向pH=13的氢氧化钠溶液中不断加水稀释 | |
| D. |  化学反应中,原子总数随时间的变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图所示,实验Ⅱ是电解水的装置.
如图所示,实验Ⅱ是电解水的装置.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题


查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 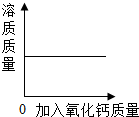 一定温度下,向饱和的石灰水中加入氧化钙固体 一定温度下,向饱和的石灰水中加入氧化钙固体 | |
| B. | 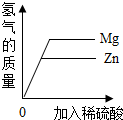 向等量的镁、锌固体中加入足量的稀硫酸 向等量的镁、锌固体中加入足量的稀硫酸 | |
| C. | 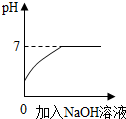 向稀盐酸中加入过量的氢氧化钠溶液 向稀盐酸中加入过量的氢氧化钠溶液 | |
| D. | 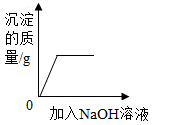 向盐酸和氯化镁混合溶液中加入过量的氢氧化钠溶液 向盐酸和氯化镁混合溶液中加入过量的氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 所得滤渣中一定含有铜和锌 | |
| B. | 所得滤渣中一定含有银和铜 | |
| C. | 所得滤渣中一定含有银、铜和锌 | |
| D. | 所得滤液中一定含有Ag+、Zn2+、Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com