
 ������ĸA��H�������л��г��������ʣ��������⡢̼�������ơ��ơ����е�2-3��Ԫ�����
������ĸA��H�������л��г��������ʣ��������⡢̼�������ơ��ơ����е�2-3��Ԫ��������� ��1������A�������׳��⣬ϡҺ�ʼ��ԣ����ƶϳ�A��NaOH��
��2����ɫ��ĩ��������������������һ����̼��̼�ȷ�Ӧ��
��3������Һ��ƿ�֪��Ӧ���к�����Ԫ�أ������ݲ����ҿ�ȼ�ó�������������˵����Ӧ���к�����Ԫ�أ�
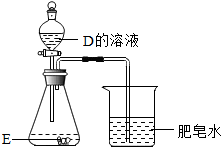
��4������������D������Һ��Ӧ����ˮ���ɿ�֪����Ӧ��Ӧ���Ǽ��̼���Σ����ɽ�F����Һ��G����Һ������ɰ�ɫ����H��֪��H��̼��ƣ������ó�F��G���������ƺ�̼���ƣ�
��� �⣺��1������A�������׳��⣬ϡҺ�ʼ��ԣ����ƶϳ�A��NaOH��
��2����ɫ��ĩ��������������һ����̼��Ӧ��Ӧ���ɵ��ʵ����Ͷ�����̼��ע��C��������������Ϊ��ĿҪ����2-3��Ԫ����ɣ�
��3������Һ��ƿ�֪��Ӧ���к�����Ԫ���ҷ������Ǹ��ֽⷴӦ�������ݲ����ҿ�ȼ���ж������������ҷ��������û���Ӧ��˵����Ӧ���к�����Ԫ�أ��ʿ��ƶ������������Dϡ���ᷴӦ��
��4������������D������Һ��Ӧ����ˮ���ɿ�֪����Ӧ��Ӧ���Ǽ��̼���Σ�F��G��H�ж�����OԪ�أ����ɽ�F����Һ��G����Һ������ɰ�ɫ����H��֪��H��̼��ƣ������ó�F��G���������ƺ�̼���ƣ�
�ʴ�Ϊ��
��1�����ռ�����ƣ���
��2��Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��3��Fe+2HCl�TFeCl2+H2����Fe2O3+6HCl�T2FeCl3+3H2O��
��4��Ca��OH��2+Na2CO3�TCaCO3��+2NaOH��
���� ������ƶ���������ʵ�Ԫ����Ϊ����������ˣ���Ϥ�������ʵ���ɡ����ʼ��仯���ɶԸ��������漰���ʵ��ƶϾ�������Ҫ�ˣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ȼ�շ�������ɫ���� | |
| B�� | ȼ��һ����Ҫ�����μ� | |
| C�� | �����ľƾ�������ȼ�գ���ʪ������ | |
| D�� | ������ȥ�����������黯���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
| A | ����H2��CH4 | �ֱ��ȼ�����ڻ����Ϸ��ָ����ձ� |
| B | ����һƿ�����Ƿ�ΪCO2 | ��ȼ�ŵ�ľ������ƿ�� |
| C | �������͵�ʯ��ˮ�䱥�� | ���������������� |
| D | ��ȥ���ֱ����ռ��е�̼���� | ��������ʯ��ˮ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| 1g������ȫȼ�ղ��� | |||
| �ų�������/kJ | CO2������/g | ����SO2������/mg | |
| ���� | 56 | 2.75 | 0.3 |
| ú | 32 | 3.67 | 11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ˮ��ե��֭ | B�� |  �ƶ����� | C�� |  Ŵ������� | D�� |  ���������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com