
【题目】己知浓盐酸(HC1 气体的水溶液)与二氧化锰可以用于实验室制取氯气(Cl2), 化学方式为:MnO2+4HCl=Cl2↑+X+2H2O
(1)X 物质为_____________(填化学式);
(2)200g 质量分数为 36.5%的浓盐酸与足量二氧化锰反应制取氯气的质量为多少___________?
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】从“丝绸之路”到“一带一路”的倡议,促进了东西方经济、文化的交流。
(1)“丝绸之路”把中国的丝绸、茶叶等传人西方,将西方的宝石等带人中国。丝绸裁剪缝制的过程是________(填“物理”或“化学”)变化;
(2)新鲜茶叶中含维生素C,其化学式是C6H8O6,C6H8O6由________种元素组成;
(3)宝石的成分复杂,其中所含的Al2O3属于________(填“单质”或“化合物”);
(4)Al2O3中Al的化合价是________;
(5)能源合作是“一带一路”的重要内容,中缅油气管道将石油和天然气输人中国。石油是由多种化合物组成的________(填“混合物”或“纯净物”);天然气的主要成分是________(填化学式),甲烷充分燃烧的化学方程式为________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文: 2020年 全国将推广使用车用乙醇汽油
乙醇,俗称酒精,化学式:C2H5OH,工业乙醇一般为无色透明液体,易燃易挥发,略带酒的芳香气味,主要有合成(乙烯水化)和酿造(玉米或木薯)两种方式生产。
酿造(固态发酵法):的制作过程主要有以下步骤: 原料粉碎——配料(原料混合)——蒸煮糊化——冷却——拌醅——入窖发酵——蒸酒(蒸馏)。
工业合成(乙烯水化法):石油裂解得到的乙烯,乙烯(C2H4)与水蒸气在磷酸(H3PO4)催化剂存在的条件下,在高压高温下可直接发生加成反应,生成酒精。
乙醇汽油是把乙醇和普通汽油按一定比例混配形成新型替代能源。按照我国的国家标准,乙醇汽油是用90%的普通汽油与10%的燃料乙醇调和而成。乙醇汽油作为一种新型清洁燃料,是当前世界上可再生能源的发展重点,符合我国能源替代战略和可再生能源发展方向,乙醇汽油是一种混合物而不是新型化合物。在汽油中加入适量乙醇作为汽车燃料,可节省石油资源,减少汽车尾气对空气的污染,还可促进农业的生产。乙醇不影响汽车的行驶性能,还减少有害气体的排放量。
车用乙醇汽油含氧量达35%,使燃料燃烧更加充分,乙醇中的氧可减少汽车尾气中初级PM2.5,在一般汽车普通汽油中加入10%燃料乙醇可减少颗粒物排放36%,而对高排放汽车可减少64.6%。次级PM2.5中的有机化合物直接与汽油中芳烃含量有关,使用乙醇取代汽油中部分芳烃可很好减少针对次级PM2.5。
据国家汽车研究中心所作的发动机台架试验和行车试验结果表明,使用车用乙醇汽油,在不进行发动机改造的前提下,动力性能基本不变,尾气排放的CO和HC化合物平均减少30%以上,有效的降低和减少了有害的尾气排放。
依据文章内容回答下列问题。
(1)固态发酵法制乙醇属于_____变化(填“物理”或“化学”)。在加油站加油时,打开油箱,能闻到特殊的芳香气味,从微粒的角度解释其原因是_____。
(2)下列有关乙醇汽油的说法正确的是 _____。(填字母序号)
A. 乙醇汽油是一种新型化合物
B. 使用乙醇汽油,不需要进行发动机改造
C.长期使用乙醇汽油有利于减少雾霾
D.乙醇汽油中乙醇与普通汽油体积比大约是1:9
E.使用乙醇汽油排放的尾气中不含有CO
(3)写出乙烯水化法合成乙醇的化学方程式________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如下图是钠元素和氯元素在元素周期表中的信息和四种粒子的结构示意图。

请回答下列问题:
(1)钠原子的相对原子质量是_____。
(2)阴离子的结构示意图是_____(填字母),其离子符号为_________。
(3)A和C两种粒子的___________________相同,所以它们具有相似的化学性质。
(4)BD两种粒子形成的化合物的化学式为____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】浙江大学团队研制出新型铝——石墨烯超级电池,充电 5 秒通话 2 小时。它的正极是石墨烯(石墨中剥离出来的单层碳组织)薄膜,负极是铝。把两片电池串联在一起,就 能点亮一组 LED 灯(由 0、C 等元素组成的环氧树脂)。如右图所示,请回答下列问题。
(1)图中标示的物质中,属于非金属单质的是 _______, 铝离子的结构示意图是 _____.
(2)超级电池在达到使用寿命期限后要回收处理,既是为了资源再利用,也是为了_______.(写一点)。
(3)已知铝像铁一样可以在氧气中燃烧生成氧化物(氧化 铝),请写出铝在氧气中燃烧的化学反应方程_______
(4)从铅酸蓄电池到新型铝——石墨烯超级电池,你得到的启示是 _______。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】美国普度大学研发出一种利用铝镓合金制备氢气的新工艺,流程如下图所示:
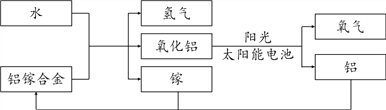
(1)氧化铝(Al2O3)制得铝的反应中,铝元素的化合价______(填“升高”“降低”或“不变”)。
(2)氧化铝中的氧元素来自于__________。
(3)上述过程中,涉及到的氧化物有__________。
(4)氧化铝可以借助太阳能电池重新变成氧气与金属铝,该反应的反应类型是__________(填“化合反应”或“分解反应”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自然界中二氧化碳的循环过程如图所示:
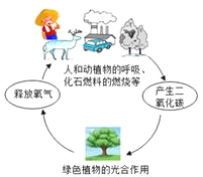
(1)吸收大气中CO2的环节是________。
(2)由于人类消耗化石燃料的增加和森林的乱砍滥伐,使空气中CO2的含量上升,从而导致_______增强,全球气候变暖。我们需要倡导“低碳”生活.要降低二氧化碳的排放,可采取的措施有:__________。
(3)科学家研究得到:海洋是吸收大量CO2的地方。如果工业生产产生的CO2排放量继续以目前速度增加,海洋将成为“酸化的海洋”。请写出酸化原因的化学反应方程式:_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列实验示意图回答相关问题:

(1)实验中的错误是_______________;
(2)图中所表示的读数为_________g;称取氯化钠的实际质量为_________g;小红在称量16 g氯化钠中,正确操作,天平指针偏向右边,小红接下的正确操作是_______。
(3)小红在称量16 g氯化钠中,称量实际值小于16 g,导致这一结果的原因是____(填字母)
A.天平指针偏左称量 B.天平指针偏右称量 C. 称量前游码示数为1 g 且天平平衡称量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在老师的指导下,某学习小组利用如图1所示装置对氯酸钾(KClO3)制氧气进行了深入的探究学习.
资料:
①KClO3的熔点约为356℃,MnO2的分解温度约为535℃.用酒精灯物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指KClO3和MnO2混合物中,KClO3和MnO2的质量比;
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图及不同配比时氧气浓度随温度的变化示意图如图:
(1)分析图2,KClO3分解温度___________(填“高于”、“等于”或“低于”)其熔点.
(2)分析图3,KClO3分解温度随物质配比变化的规律是__________当物质配比为1:2时,KClO3分解温度约为________℃.
(3)为证实MnO2的催化作用,小组同学利用如图4装置进行如表所示的实验:
步骤 | 实验操作 | 实验现象 |
Ⅰ | 检查气密性 | 气密性良好 |
Ⅱ | 分别在“Y”形管两侧支管中加入少量MnO2和KClO3,塞紧橡皮塞. | 没有明显现象 |
Ⅲ | 分别先后加热MnO2和KClO3,用带火星木条放在导管口.加热__________(填“左”或“右”)侧支管后,带火星木条复燃. | 木条长时间才能复燃 |
Ⅳ | 冷却后,将“Y”形管左侧支管中部分MnO2混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口. | _____________ |

步骤Ⅳ的实验现象能否说明MnO2是KClO3分解的催化剂?___________(填“能”或“不能”),除催化剂外,影响化学反应的速率的因素还有___________和__________等.
(4)分析图2,在KClO3分解前,传感器得到氧气浓度降低的可能原因是____________.
(5)将29.4gKClO3和MnO2混合物以5:1配比加热至完全反应,如图5中?的值应为_________
A.4.9 B.9.6 C.14.9 D.19.8.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com